陽明交大創新醫材轉譯研發中心在醫學與工程兩校強強結合併校後成立,不到一年,便取得醫材製造/販賣兩項許可證,擁有多達8家的合作醫院的醫療資源,還是國內唯一擁有TAF認證實驗室聯盟的大學,能夠產出接軌國際監管單位的報告,讓創新醫材邁向國際市場。研發中心也秉持「從臨床需求出發,臨床應用落地」的核心理念,把難以商業化的Biotech化為Medtech!
撰文/李林璦
陽明大學與交通大學於2021年2月合校後,首任校長林奇宏一上任便推出「一樹百穫」計畫,在10年願景中,強調跨領域、產學共創等概念,融合陽明豐沛的臨床醫學資源和交大領先國際的工程研發技術,相互激盪、強強聯手,於今年1月設立了一級校級研發中心──「創新醫材轉譯研發中心」。
在2021年5月《醫療器材管理法》正式從《藥事法》抽離後,林奇宏大力支持創新醫材轉譯研發中心申請取證,並於今(2022)年8、9月相繼獲得醫療器材販賣商及製造商兩項許可證(醫用軟體及植入物),這是《醫材法》成為專法一年後,為創新醫材所開啟的新扉頁!
代表著學研單位不需再委託擁有藥商許可執照的製造業者作為許可證持有者,也解除了歷盡艱辛誕生的產品卻無法擁有許可證的困境,大幅提高學研單位與軟體業者投入創新研發的動機。
創新醫材轉譯研發中心主任林峻立教授強調,「一級研發中心的高度代表直接對校長負責,並可直接跨陽明與交大兩校區進行整合,從校級的層級推動創新醫療器材從研發走向臨床落地。」
智慧、精準趨勢夯 轉型升級、創新法規成關鍵挑戰
陽明的醫學工程學系是全臺國立大學中第一個創辦,醫工研究所從1984年成立至今已有近40年的歷史,不僅學生遍佈國內外醫材產業,也孕育出多項創新醫材取得美國食品藥物管理局(FDA)、歐盟CE及臺灣食藥署(TFDA)認證上市,並應用於當今的臨床治療上。
林峻立指出,臺灣政府從2009年南科的齒科醫療器材研發計畫開始,便持續推動醫材產業發展,從2015年切出一個分水嶺,之前大多專注於發展「利基醫材」,諸如臺灣已經推動10幾年,趨於成熟的人工牙根、隱形眼鏡、血壓/血糖計、輪椅/輔具/病床、輸液管/針筒/轉接管、手套/口罩/紗布/繃帶等。
隨著時代演變,臺灣從早期以生產醫用耗材為主走向中階居家醫材產品,跨過2015年的分水嶺之後,臺灣朝向「精準治療」與「智慧醫療」發展,以往的利基醫材也進一步結合資通訊技術、大數據、人工智慧技術、高階生醫材料等,朝向智慧及精準醫療邁進,就能讓應用從診斷、治療,向前擴及疾病預防、健康促進,朝「2030 全齡健康」的目標邁進。
林峻立表示,不同類型的醫材所面臨的挑戰完全不同,對於已經發展成熟的利基醫材來說,已跨越法規、製造及查驗登記的關卡,如何臨床落地、行銷佈局、蒐集大數據讓廠商再升級是目前主要的挑戰;而對於精準醫療、智慧醫療來說,產業還正在萌芽起步,同時還要隨著時代變化快速發展,因此,主要挑戰在於法規、制度的建立以及ICT廠商的轉型認證。
「面對不同類型醫材所需的研發轉譯、升級轉型、跨領域合作、產學鏈結時,創新醫材轉譯研發中心也運用健康醫療資源的整合,鏈結與彌平醫學和工程間的鴻溝,與產業界、醫界一同建構醫材產業聚落。」林峻立說。
攜手8大醫院 從臨床出發臨床落地
林峻立指出,陽明與交大合校後,有了ICT產業的支持,最大賣點是精準醫療與智慧醫療,但最大的挑戰是,該如何把難以商業化的創新研究(Biotech),進入到以臨床市場需求為主的創新開發(Medtech),不能只是單純將工程技術應用到生物醫學。
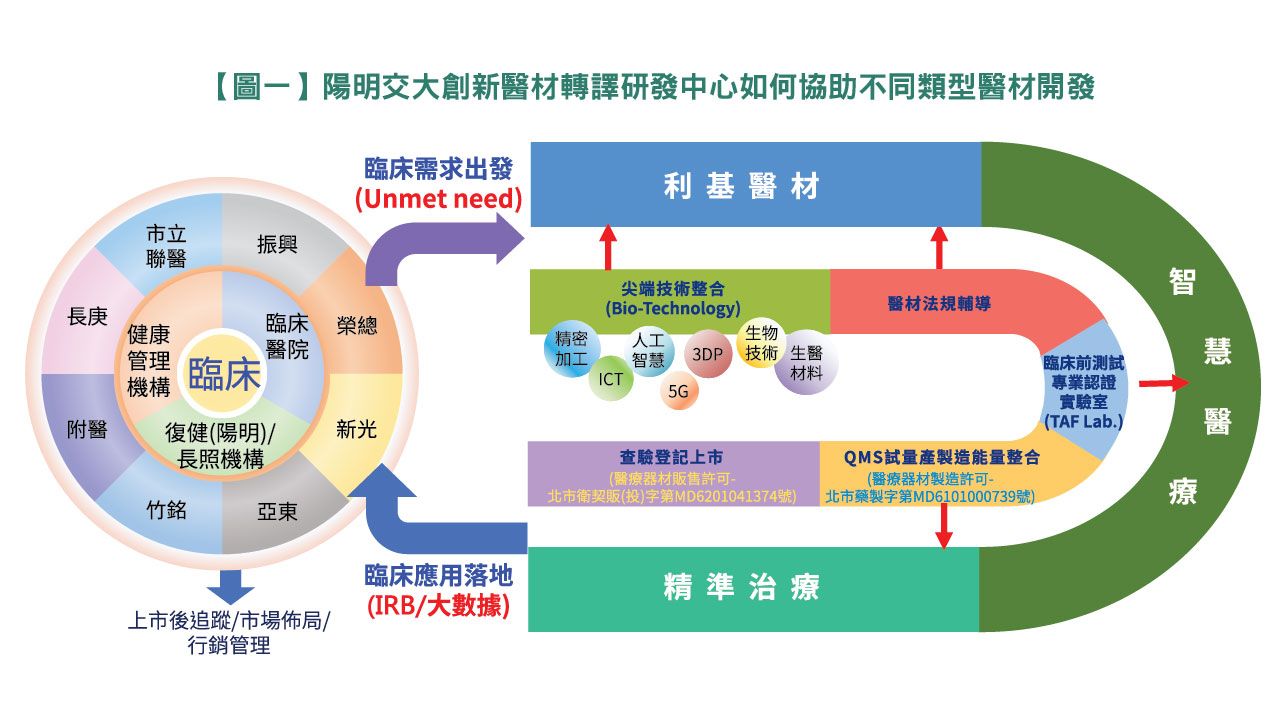
因此,創新醫材轉譯研發中心的核心目標為「從臨床需求出發,臨床應用落地」,協助老師們從「臨床需求端」著手,經歷工程技術的適用性及整合評估、法規檢測/臨床前測試(或臨床測試)的驗證,產業醫療器材製造業者品質管理系統(QMS)/GMP建立及試量產等階段工作後,才能進行查驗登記取證,取證後接著進入臨床落地應用測試,再進一步蒐集臨床回饋或大數據分析,醫材產品才能真正地進入市場並有效地布局及行銷,走到落地的最後一哩路。
林峻立坦言,我們希望向過去發展利基醫材的經驗取經,讓智慧醫療跟精準醫療可以不必繞遠路、快速地走向臨床應用。以往在發展利基醫材時,很多時候的臨床需求可能是學校老師自己發想,獨自研發,等到產品出爐再去進行臨床測試,但到了臨床卻遇到重重阻礙,因此,首要條件就是需求必須要從臨床出發!
「陽明交大也已經與榮總、振興、新光、亞東、衛福部立醫院、臺北市立聯合醫院、竹銘醫院、陽明交大附設醫院等多家醫院,以及健康管理機構、復健/長照機構簽訂結盟合約,讓醫療器材進入臨床試驗,並在不同醫療領域中建立臨床數據共享資料庫。」林峻立說。
全臺唯一校內TAF實驗室 國際級標準接軌FDA、CE
除了建構完善「以終為始」的臨床環境,在醫材研發的過程中,法規、安規可說是最為關鍵,林峻立也指出,創新醫材在進入醫院場域時,醫院方都希望要取證後才能進入臨床,而複雜的法規文件、流程也常是老師們新創醫材所面臨的難關之一。
因此,在醫材進入臨床前的法規技術測試方面,陽明交大是國內唯一擁有TAF認證實驗室聯盟的大學,具有4個ISO 17025認證實驗室,包含生醫工程分析實驗室(醫工系林峻立教授)、游離輻射檢測實驗室(醫放系陳志成教授)、生醫智慧計算實驗室(醫工系陳右穎教授)以及食品檢驗分析實驗室(醫放系吳杰教授),可以提供校內教授以及校外廠商進行醫療器材、醫療放射、醫療軟體及機電介面、食品安全等領域的測試。
林峻立解釋,事實上,TAF實驗室在醫材開發的各個階段都扮演關鍵角色,在開發階段時,就能依循上市法規要求,隨即針對雛型品進行相關測試,加速產品研發時程;在醫材上市前,也必須透過TAF實驗室產出功能性測試來驗證產品之安全性、有效性。
「校內擁有TAF實驗室的好處在於,相較以往送外部檢測機構,老師可以非常即時地透過測試報告來修改醫材,且TAF實驗室的檢測報告具國際標準,可以用於申請美國FDA或歐盟CE認證,也是後續產品送件QMS與查驗登記必備文件。」林峻立指出。
陽交獲醫材製造/販售證 打開醫療軟體大門
2021年《醫材法》從《藥事法》獨立後,現在,學研新創團隊可以在學校,從設計開發走到完成QMS、雛型驗證、品質文件的管制等等,最後再委託製造公司進行生產或量產。
陽明交大也在8、9月取得醫療器材製造商執照以及販售業許可證。林峻立指出,醫材法獨立後,讓「設計」跟「製造」分開,對於還沒建構GMP系統的新創團隊是一大福音,也有望讓創新醫材的價值、技轉金額提高,使更多產品走向商品化。
林峻立強調,這項法規尤其對於「醫療軟體類」醫材開了一扇大門,醫材種類繁多,多數脫離不了還是要進入具有「工廠登記證」的工廠進行生產製造,但是,醫療軟體不太需要一個真正的「工廠」進行生產製造,在經過軟體功能驗證後,不須找尋具有相對應QMS品項的軟體技術製造廠商,即可進行製造及查驗登記。
像是陽明交大生物醫學暨工程學院副院長吳育德團隊就與臺北榮總及臺中榮總合作,利用超過2,000筆磁振造影資料,其中包含了20萬張二維影像,結合影像處理技術及深度學習技術,開發出用於判別聽神經瘤/腦膜瘤/腦轉移瘤術前放射治療療效預測的「DeepBT腦瘤智慧精準醫療系統」。
該系統運用獨特的雙通道U-net深度捲積神經網路進行三維自動腦瘤圈選,不僅能克服影像軸向與平面解析度不同、不同類型腫瘤數量不均,體積大小位置不一、術前術後腫瘤變化與對位等問題,還能計算多時間點的腫瘤體積變化,提供醫師術前療效預測。
「該軟體目前正積極進行軟體功能驗證,預計明年將申請衛福部醫療軟體的查驗登記,核准後,陽明交大已取得醫材販售證,便可直接技轉或是販售給相關的醫學中心。」 林峻立說明。
「紮實地走了一輪流程後,更了解到從臨床出發的重要性。創新醫材轉譯中心希望先協助團隊們克服法規、建構各種類型產品的QMS,促進更多醫材商品化,取得查驗登記證,未來能更進一步跨入臨床應用,邁進國際市場。」林峻立說。
林峻立也期許,未來,透過創新醫材轉譯中心能培養出更多學生投入創新醫材研發,並鏈結陽明交大的生醫與工程、整合合作醫院的醫療資源,逐漸凝聚形成新興醫材產業聚落,為臺灣醫材產業注入巨大的研發轉譯能量。
長年深耕創新醫材 續攻癌症、腦科、高齡醫學
雖然創新醫材轉譯中心在合校後成立,但陽明與交大早有長久的醫材發展歷史、量能,其累積的深厚根基也是創新醫材轉譯中心首要瞄準的領域,也正是目前全球醫材發展上的趨勢。
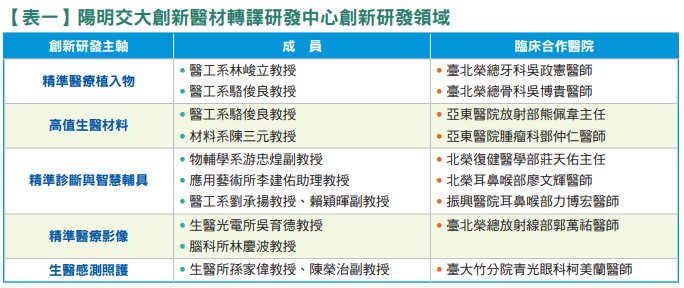
林峻立表示,從陽明大學時代開始,腫瘤癌症、腦科學及高齡醫學等領域便極具代表性,創新醫材轉譯中心從這些領域出發,並結合精準與智慧醫療,發展出精準醫療植入物研發、高值醫材與仿生材料研發、精準診斷與智慧輔具研發、精準醫療影像技術研發、生醫感測照護系統研發等主題。
林峻立舉例分享,陽明交大已開發出臺灣首部針對吞嚥困難/障礙與舌肌力量測系統,不僅可偵測吞嚥能力,還能搭配App進行復健。
該舌壓計是林峻立與高雄醫學大學口衛系教授劉秀月,高雄小港醫院院長郭昭宏及神經內科醫師陳俊鴻共同開發,團隊先收集了1,000位以上的高齡者舌壓數據,建構出臺灣本土高齡者舌壓的常模數據庫。
接著,以舌壓計搭配App,醫師可檢測患者舌壓是否落在常模中,同時可設定復健指令與目標,達到量測與復健的效果,目前已通過QMS並已取得衛福部TFDA查驗登記通過,並於亞東醫院進行腦中風患者吞嚥障礙復健治療等研究。


林峻立期許能協助團隊克服法規、取證、商品化,並培養更多創新醫材人才、凝聚新興醫材產業聚落,為臺灣注入巨大的研發轉譯能量。(攝影/羅翊方)
>>本文刊登自《環球生技月刊》Vol. 100









