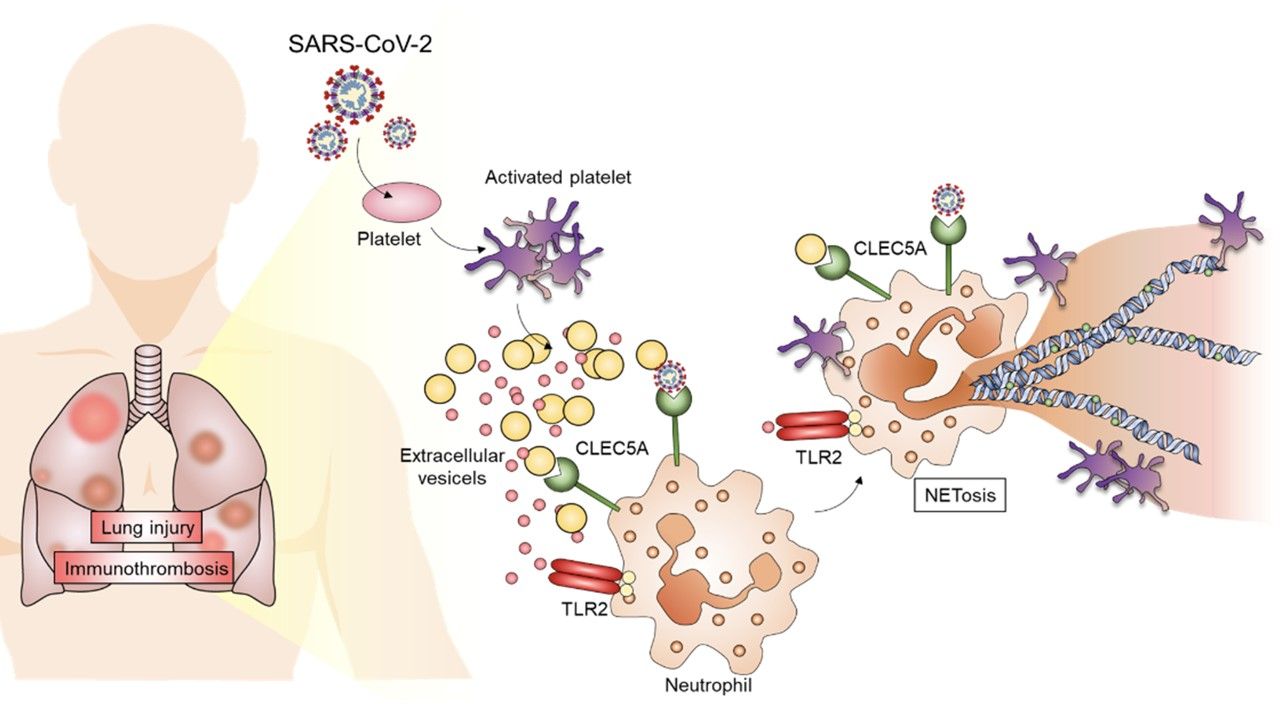
近期,中研院基因體研究中心特聘研究員謝世良與博士後研究學者宋佩珊研究團隊,揭露COVID-19的病原體SARS-CoV-2容易引發血栓的關鍵原因。研究發現,SARS-CoV-2會活化血小板以放大發炎反應,進而產生血栓,只要阻斷嗜中性白血球表面的兩個受體CLEC5A和TLR2,就可以緩解血栓症狀、減少血管內凝血以及發炎。研究成果已發表於《Journal of Biomedical Science》期刊。
謝世良與宋佩珊長年研究宿主與病原體的互動和免疫調控作用的機轉,已發現登革病毒、流感病毒、B型肝炎病毒等多種病原體致病的關鍵先天免疫受體,並在去年創立三喬醫學科技,致力於將此學術研究成果轉譯至臨床應用。
近來多項研究顯示,COVID-19所引起的血栓數幾乎是流感的9倍,而且影響所及有可能是終身,即使從COVID-19康復,之後出現肺栓塞、呼吸道症狀的機率,仍比未曾染疫者多了一倍。不過,SARS-CoV-2在肺臟裡引起血栓,堵塞微血管的原因,至今尚未有定論。
宋佩珊表示,收集COVID-19急性期患者的血液檢體時發現,血液中含有高量的胞外囊泡(Extracellular vesicles, EV),且這些胞外囊泡大多從血小板而來,顯然與血小板受到病毒活化有關。血小板被活化後,釋放大量地胞外囊體去刺激嗜中性白血球,產生大量的嗜中性白血球胞外捕捉網(neutrophil extracellular traps, NETs)及自殺式的細胞死亡(NETosis)。
宋佩珊說,雖然過去的報導指出NETs有助於病菌的清除,但是近期許多COVID-19研究則顯示,病人體內過多的NETs會引起免疫血栓(immunothrombosis),甚至是嚴重的血管內栓塞。這些肺部微血管阻塞,會導致肺部及其他器官缺氧,進而造成全身性損害。
為了探究誘導NETs形成的機制,研究團隊分別採取健康受試者和COVID-19病患的胞外囊泡,進行質譜儀(Mass spectrometry)分析。結果指出,SARS-CoV-2感染引起的胞外囊泡表現了大量血小板相關蛋白,且具有多種與白血球去顆粒性(degranulation)以及血小板活化凝集的蛋白,顯示COVID-19病人血液中血小板劇烈活化。
研究團隊進一步將這兩種不同來源的胞外囊泡與嗜中性白血球培養,比對它們誘導NETs形成的能力。結果顯示,健康對照組的胞外囊泡無法誘導NETs形成,但COVID-19患者的胞外囊泡誘導了強大的NETs形成,而阻斷嗜中性白血球表面的兩個受體CLEC5A和TLR2,能夠抑制NETs形成。
在動物實驗中,研究團隊發現感染SARS-CoV-2病毒的小鼠們,感染3~5天後,在肺部會有大量的NETs產生以及嚴重的細胞浸潤;反觀CLEC5A和TLR2基因剔除的小鼠,發炎以及細胞浸潤的情況大幅降低。
基因體研究中心表示,這些實驗數據證實,血小板中胞外囊泡的數值與SARS-CoV-2感染和血栓栓塞密切相關,因此,抑制血小板活化可能成為未來減輕病毒引起的肺部發炎反應的新策略。
謝世良表示,來自病毒活化血小板釋放的胞外囊泡(EVs from virus-activated platelet, aPLT-EVs),是促進發炎反應的內在危險因子(endogenous danger signal),而且是經由CLEC5A和TLR2傳遞訊息。
謝世良表示,降低COVID-19急性後遺症的發病率,CLEC5A和TLR2是有希望的治療靶點,可在未來減輕血栓炎症,並降低急性後,產生COVID-19後遺症的風險。
謝世良指出,團隊不僅在先前的研究發現,阻斷CLEC5A和TLR2成功壓制登革病毒引起的出血性休克,新研究也為治療COVID-19血栓併發症開啟新的方向。研究團隊將會繼續循線探索,找出更多治療疾病的新療法。
參考資料:https://www.genomics.sinica.edu.tw/index.php/tw/news/lastest-news/689-clec5a-tlr2-sars-cov-2
論文:https://jbiomedsci.biomedcentral.com/articles/10.1186/s12929-022-00832-z
下一篇