
林口長庚醫院院長陳建宗(攝影/巫芝岳)
林口長庚醫院院長陳建宗致詞表示,長庚是臺灣最大且領先的醫院之一,擁有約3700床,員工超過1000人,致力於突破創新、獲取醫療新知外,更重視患者照護,期許透過舉辦國際論壇促進更多知識與經驗的交流。
精準、安全放療新未來!Vincent Grégoire:CT引導、AI圈選、3D影像

法國知名癌症醫療機構Léon Bérard中心放射腫瘤科主任Vincent Grégoire(攝影/巫芝岳)
Vincent Grégoire從放射治療的起源開始分享,他指出,X射線是由Wilhem Conrad Rontgen於1895年發現,1919年到1946年時,居禮研究所(Institut Curie)運用X射線治療喉癌患者只有25%患者達到臨床治癒。
不過,從1960年代的平面式規劃(2D),到1990年代的三度空間順形放射治療(3D-CRT),進一步發展到2000年代的強度調控放射治療(IMRT),在頭頸癌的局部放療中,疾病獲得控制的比率已經從1985年的27%,進展到2013年的84%,此外,由於IMRT可以更精準的治療,可保留患者腮腺(parotid)、吞嚥肌肉的功能,不僅可以更精準的定位癌細胞,也改善了患者的治療與預後。
Grégoire指出,在1980年代,他們團隊發表了體外放射治療(EBRT)指引共識50 (ICRU 50),也成為第一份紀錄質子治療(proton beam therapy, PBT)的指引,後續也陸續發表重粒子治療指引。
他表示,影響放射治療的關鍵參數包含:腫瘤的位置、淋巴結的狀態、患者的合併症、以及患者的選擇等等。未來,Grégoire指出,2025年後的頭頸癌放療,需要重新檢視腫瘤的範圍、體積的劃分,重新描繪危及器官(Organ At Risk, OAR)的範圍,重新評估放射劑量。
他表示,在頭頸癌的放射治療中,也許不需要每次都治療頸部兩側,研究發現,若根據頸部兩側淋巴結浸潤的數據調整放療,發現雙側照射與單側照射聯合免疫檢查點抑制劑PD-L1相比,無惡化存活期(PFS)並沒有顯著差異,顯示能夠在有療效的同時也降低復發率,並延長患者的存活期。
此外,Grégoire也運用單光子電腦斷層掃描(SPECT)/電腦斷層掃描(CT)來引導選擇性的照射頭頸癌淋巴結,患者的生活品質更好、吞嚥困難、口乾舌燥的狀況也較少。
Grégoire指出,結合斷層掃描、人工智慧(AI)輔助標註、內視鏡模擬3D虛擬影像,是放療的未來,不僅可以節省標註時間,也能成為更安全、毒性較小、預後較佳的新療法。
Søren M. Bentzen:細究放療等效概念發展 「相對生物效應」有賴臨床數據累積

馬里蘭大學醫學院(University of Maryland School of Medicine)教授Søren M. Bentzen(攝影/李林璦)
Søren M. Bentzen表示,經歷Leopold Freund 1897年首次以放射線治療多毛症,到Tage Sjogren在1899年首次用放療治療癌症之後,直到1910~1920年代,人們才開始注意放療之後出現的副作用,因此開始重視放療的劑量測定(dosimetry),並試圖研究能有效控制腫瘤、且病人可耐受的理想劑量,以及透過發展更多不同類型放療,來準確評定出使用有效且安全的劑量。
Bentzen接著介紹了最早從Frank Ellis於1969年提出的「放射線對皮膚影響的等效曲線:D=NSD N^0.24T^0.11」(D=劑量、N=治療次數、T=治程天數、NSD=標稱標準劑量),經後人多次修正,最終如何發展出當今的等效劑量公式:
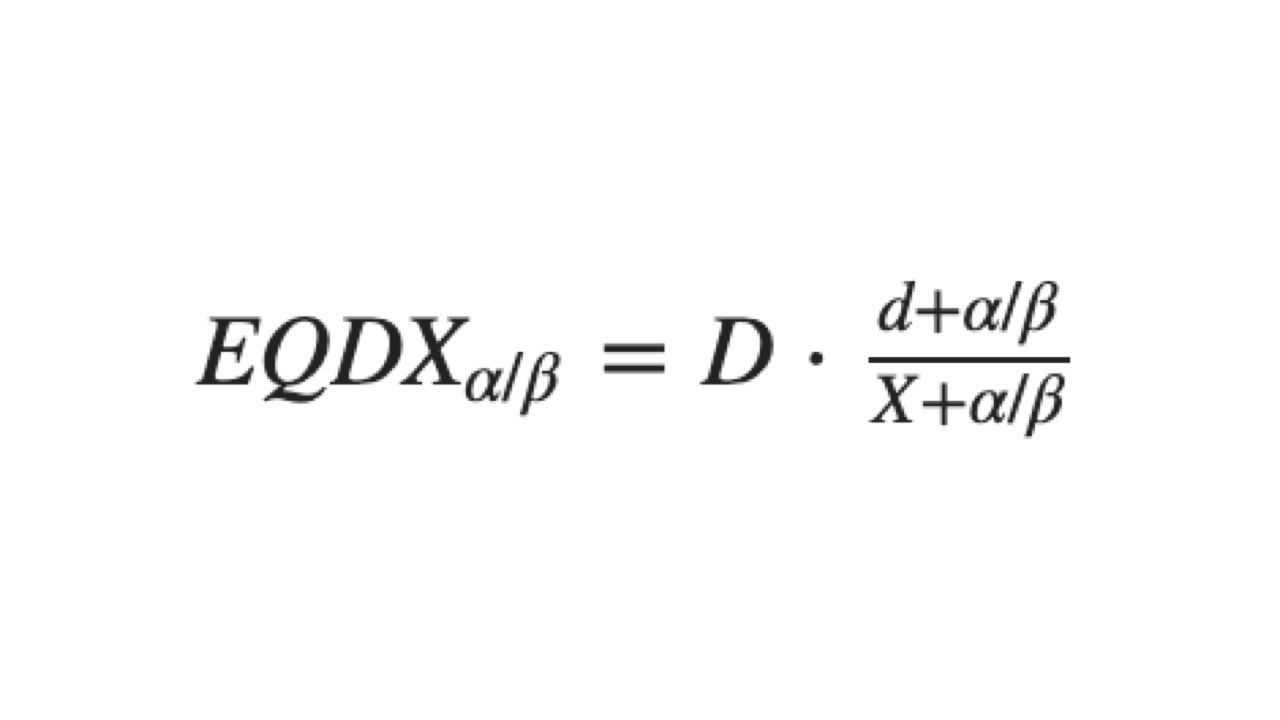
Bentzen說明,「等效」的定義為:在不同dose-time fraction (劑量和治療時間上的變化)、和/或不同劑量-速率模式(dose-rate pattern),和/或是空間分佈(space distribution)、放療劑量下,兩項放療在一種臨床評估指標(endpoint)上能達到等效。
Bentzen表示,然而由於射線種類不同,對生物體產生的效應也不相等,針對這項「相對生物效應」(relative biological effectiveness, RBE),科學家也已提出相應的數學模型;但他也表示,臨床上實際的狀況,仍會取決於實際的評估指標,而不應僅以單純帶入公式產出數字進行統計,因此,要能準確運用一項新的放療,仍有賴更多臨床經驗累積。
對於研討會中,多次討論到AI在放療中的相關應用,Bentzen認為,AI仍有賴於正確的大數據庫建置,且由於對病人重要的決策,仍應由醫師進行,所以AI或許能幫協助節省工作時間,但絕對無法取代醫師。
此次研討會也獲得多家廠商贊助,包括:科技公司華碩電腦股份有限公司、祥碩科技股份有限公司,以及開發AI智慧病理工具的捷絡生物科技股份有限公司。
(報導/李林璦、巫芝岳)









