責任編輯/王柏豪
2022年7月臺大醫院公佈臺灣首例CAR-T細胞治療10歲的血癌病童,揭示臺灣進入CAR-T細胞治療時代。除了CAR-T細胞療法,近年來多項新興藥物、療法及技術逐步發展成熟,提供醫師更多樣性的創新藥物及療法,例如抗體藥物複合體(ADC)、再生醫療(幹細胞、iPSC 等)、基因療法、核酸藥物(RNAi、ASO、mRNA等藥物)及疫苗等,使人們對重大疾病不再束手無策。
臺灣政府相繼推動之「5+2產業創新計畫」和「六大核心戰略產業」,也為精準治療發展提供助力。2021年12月公布修訂的「生技醫藥產業發展條例(生技醫藥條例)」將精準醫療、數位醫療、再生醫療、創新技術平台、新劑型製劑、CDMO等新增納入適用範圍;2022年,與基因、細胞療法相關之「再生醫療雙法」草案也正力拚送立法院審議,通過後,將有助於縮短研發至臨床使用之期程、確立分流與分級管理、完善產業鏈並幫助細胞治療技術到製劑之銜接。
在臺灣精準治療發展萬箭齊發之際,資誠聯合會計師事務所(PwC Taiwan)與財團法人生物技術開發中心(DCB)共同合作出版《2022 PwC精準治療之發展現況與趨勢》產業趨勢研究報告。透過深度訪談及問卷調查的方式收集精準治療領域領袖之專家觀點,總計有16位產業專家深度訪談及81份企業及專家問卷調查回饋意見。
資誠聯合會計師事務所會計師暨生醫產業協同負責人游淑芬表示,依據前述意見,研究團隊針對精準治療產業發展成功關鍵,分別從六大面項,包括:法規建立、產業環境、人才培育、供應鏈建構、公私協力推動及健保給付等,提出六大建議要點供各界參酌。
建議一:加速再生醫療與數位治療產品法規建立
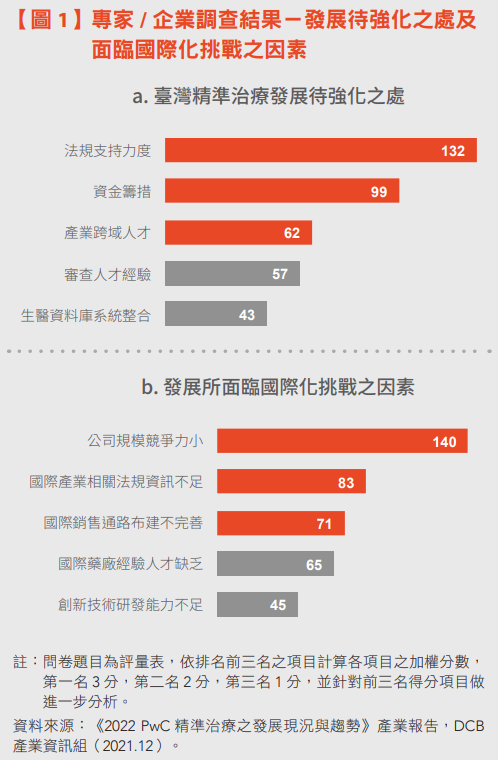
產業界與專家認為臺灣發展精準治療待強化之處,首位為「法規支持力度」(見【圖1-a】),對於臺灣精準治療產業進一步邁向國際市場,「國際產業相關法規資訊不足」(見【圖1-b】),也高居第二大挑戰。可見,業界對於法規政策是否能幫助新興治療技術發展尤為關注,重要性不容忽視。。
游淑芬建議,期待未來更增加因應再生醫療與數位治療所研議的創新審查機制,加速相關產品上市。如「再生醫療雙法」草案已納入日本再生醫療法規之精神,縮短上市前人體試驗時間,並加強上市後監測,或是參酌美國採用數位治療產品預認證機制,精簡上市審查流程。
建議二:協助建構投資與併購友善環境
「資金籌措」為產業界與專家認為臺灣精準治療產業發展待強化之處第二重要的議題(見【圖1-a】)。
游淑芬認為,為助益產業發展,政府宜協助建立不同階段企業所需之資金挹注,結盟國家級創投引導國際資金,並隨著企業逐漸成熟,資本市場扮演成長路上公開募資的重要舞台。
目前,臺灣證券交易所(證交所)已於2021 年第三季開放創新板上市申請,改採市值為上市指標並免除獲利條件。證交所為加速扶植新創企業及早進入資本市場,降低募資成本,進一步於2022年9月調降創新板的上市市值標準,其中第一類上市市值從新臺幣15億元降為10億元,營收條件由最近四季財報合計不低於1億5千萬元,調整為1億元門檻;第二類生醫類市值門檻由30億元,同步調降為20億元,申請轉板年限則由上市掛牌日起屆滿2年縮短為1年。
另一方面,證券櫃檯買賣中心開放的戰略新板,採用簡易公發制度加速企業邁向資本市場,截至2022年10月,已有樂迦再生、大江基因、台寶生醫及宏碁智醫四家生醫公司登錄。
游淑芬指出,企業發展成熟階段,往往需要透過併購或結盟合作以建立規模。如保瑞藥業連續併購日商衛采、美國Impax旗下益邦製藥、GSK加拿大及伊甸生醫等國內外製藥廠房,並於2022年6月宣布以60億元收購安成國際藥業公司,展現臺灣生醫企業逐漸採用併購策略擴大版圖,打造生醫產業規模。
建議三:完善人才培育配套措施
「產業跨域人才」為產業界與專家認為臺灣精準治療產業發展待強化之處第三重要的議題,此外,「審查人才經驗」為臺灣待強化之處第四名。 (見【圖1-a】)
對此,游淑芬指出,針對精準治療發展,需要多元專業且領域跨幅廣闊之人才需求,宜採育才與攬才措施雙管齊下。「企業要思考多元化的育才與攬才措施,打造臺灣專業及跨域人才庫。」她強調。
她建議,育才方面,期待整合產官學研醫力量進行人才培訓計畫,並落實教育訓練與場域試驗並進。
如國科會自2013 年起進行「臺灣生醫與醫材轉譯加值人才培訓計畫」(SPARK),引入美國生醫聚落資源培育國際級人才;國家生技研究園區於2021 年引進中研院、生技中心、醫藥品查驗中心、生技產業深耕學院與國際大藥廠,並已培訓超過400 位實務人員;教育部資訊及科技教育司(資科司)自2022年起辦理為期4 年的「精準健康跨領域人才之培育計畫」,培育高階智慧健康產業或多元生醫、生農人才。
攬才方面,全球生醫產業大搶人才,除了薪資待遇,強化員工對企業認同度成為攬才關鍵。
目前,臺灣施行新版生技醫藥條例,其中給予生醫高階專業人員之獎酬、技術入股或執行認股權憑證取得之股票,可享緩課所得稅擇低課稅優惠。該租稅優惠提供誘因,讓員工成為股東,進一步共享企業未來發展成果。
建議四:建構關鍵供應鏈設施與國際生醫招商平台
對於臺灣精準治療產業進一步邁向國際市場,面臨的首要挑戰為「公司規模競爭力小」,「國際銷售通路布建不完善」列為第三(見【圖1-b】)。
游淑芬表示,這顯示生醫產業急需各界投入一同強化供應鏈體質,並強化招商平台以吸引國際大藥廠合作。
她舉例指出,COVID-19 疫情衝擊帶動全球核酸藥物、基因與細胞療法等新興生技產品市場成長,這些產品需要高技術門檻與複雜的生產流程,刺激委外生物製造市場的快速成長。臺灣可思考扶植具高技術門檻的mRNA 核酸藥物、ADC藥物、異體細胞治療產品技術,以切入全球產業利基。
目前,在2022行政院生技產業策略諮議委員會議(Bio Taiwan Committee, BTC)上,行政院副院長沈榮津已表示政府將帶頭投資CDMO (Contract Development and Manufacturing Organizations,委託開發暨製造服務),建立自己的韌性產業鏈。
此外,財團法人生物技術開發中心亦宣布規劃成立以核酸藥物為主的CDMO新公司,展現政府推動臺灣生醫在地化生產的決心。
建議五:公私協力推動生物數據平台商業化應用
游淑芬表示,「生醫資料庫系統整合」為產業界與專家認為臺灣精準治療產業發展待強化之處排名第五(見【圖1-a】)。
不過,隨著政府對精準治療的重視及政策推行,已於2019 年建置「國家級人體生物資料庫整合平台(National Biobank Consortium of Taiwan)」。依據衛福部資料,截至2022年9月已有32家機構加入平台、收錄58萬筆資料、並已有17間醫院完成醫療資訊共同模式建置,並設立單一運用申請窗口。
此外,依據2022年BTC會議委員總體觀察與建議,將參考英國人體生物資料庫(UK Biobank)模式,成立兼具公益與營利的全球性健康大數據公司。
但游淑芬進一步建議,期待加速資料庫應用於精準治療產業發展,以明確、透明化與標準化之數據利用機制促進商業化應用。
建議六:創新醫藥和診斷產品納入健保給付
游淑芬表示,在研究團隊進行專家訪談中,有三成以上產業界與專家建議創新醫藥和診斷產品於健保給付需更加積極開放,以鼓勵業者推動更多創新產品的研發,並讓各界願意投入資金維持豐沛研發資源。
她表示,在亞洲,如韓國及日本等衛生主管機關以部分負擔(Copayment)方式,將癌症等重大疾病NGS檢測納入健保給付,以輔助精準治療方案擬定與加速精準治療產品開發。臺灣健保近年也已給付如肺癌標靶藥Tagrisso 的用藥前EGFR 檢測,以及癌症免疫藥物的PD-L1 檢測。
游淑芬特別指出,產業界與專家企盼「健保沙盒」之試行,能對已通過食藥署核准之創新產品,如採用NGS基因定序於伴同式診斷,或突破性創新之抗體藥物、再生醫療、基因療法、核酸藥物及疫苗等,在健保平台試用一定時間,經成本效益分析再行考量正式納入健保,以累積更多真實世界數據與證據(RWD/RWE)幫助未來產品開發。
游淑芬強調,精準治療是國家韌性之關鍵,盼臺灣能針對影響全球健康之重大疾病、開發創新療法,以達到個人化醫療與全人精準健康願景。
更期待上述六大建議要點,能進一步帶動各界投入精準治療之發展,建構臺灣生醫生態系韌性,在變動的環境下保持永續成長動能。
游淑芬為臺灣大學EMBA會計與管理決策組碩士,會計師執業期間輔導多家生技公司從新創設立、規模茁壯至上市櫃並成為業界巨擘。專長包含股票上市櫃之規劃輔導、內控制度、財務會計準則和審計準則之理論與實務、以及企業併購組織架構重整、交易流程及財務規劃諮詢等專業。
資誠一直以來十分關注精準醫療的相關議題,2018年發表精準醫療發展現況與趨勢報告、2020年發表數位健康大未來報告,資誠認為精準預測、精準檢測、精準診斷、精準治療與精準照顧五大項目將是未來各個產業的成長重心。
此次研究從國內外政策、法規市場與案例著手,希望透過調查來協助臺灣生醫產業找到自身的利基定位跟商業模式,並將與財團法人生物技術開發中心共同合作出版《2022 PwC 精準治療之發展現況與趨勢》報告。
除此之外,資誠亦協助生技醫療業者從設立、營運、募資、申請補助等各階段提供財稅、會計、法律及智財等專業服務,並長期對國際及臺灣產業布局進行深度調查,為臺灣生技醫療產業提供最佳解決方案。
>>本文刊登自《環球生技月刊》Vol. 100









