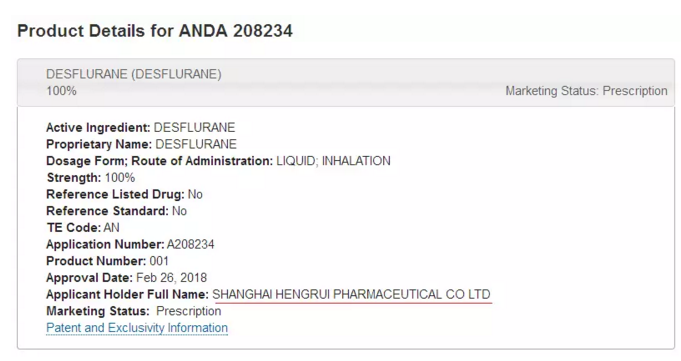
2月26日,恆瑞「吸入用地氟醚」的美國簡略新藥上市申請(ANDA 208234)獲得FDA批准。
(圖片來源:網路)
由於地氟醚屬於吸入製劑,需要原料和裝置捆綁申請,開發難度較大,此前美國市場僅有百特(Baxter)原研的Suprane(地氟醚)在1992/9/18獲批上市銷售,學名廠家極少。地氟醚是恆瑞繼環磷醯胺之後,在美國上市的第2個首款學名藥。
恆瑞地氟醚獲得FDA批准後,在市場上可以與2015年獲批的七氟醚形成協同效應。截至目前,恆瑞共有10個品種ANDA(簡易新藥上市申請,Abbreviated New Drug Application)獲得FDA批准。從劑型上看,覆蓋了口服製劑、注射製劑、吸入製劑。未來還有卡泊芬淨、卡培他濱、磺達肝葵鈉等品種的ANDA有望陸續獲得FDA批准。
2017年7月14日,恆瑞宣布「吸入用地氟醚」還分別收到了英國、德國及荷蘭藥監局簽發的批准上市的通知。國內目前也僅有百特原研地氟醚產品上市,2017年7月11日,CDE以「同一生產線生產,2017年歐盟上市」為由將恆瑞「吸入用地氟烷」的國內上市申請(CYHS1401639 )納入優先審評。
地氟醚的麻醉作用機制尚未完全明確,有報導指出,地氟醚具有對GABAA受體介導的GABA作用的增強,以及對雙孔鉀離子通道家族的TRESK的活化作用。地氟醚吸入劑適用於住院和門診成年、嬰幼兒和兒童手術患者的維持麻醉。2016年,吸入用地氟醚全球市場銷售額約2.7億美元。








