台灣科技媒體中心表示,科學家已知位於大腦第三腦室周圍的「室周器」(circumventricular organs, CVO)能直接探測血液中的滲透壓,但它究竟如何感測血液中的滲透壓、活化大腦下游的神經迴路,進而釋放抗利尿激素,此一機制始終未知。
黃朝榮與連正章團隊的台美跨國合作,在小鼠室周器中發現一群位於下視丘前緣的OVLT神經元,表現出一種叫做WNK1的蛋白質,可以感知滲透壓的上升而活化。(編按:OVLT(Organum vasculosum of the lamina terminalis,終板血管器),是一種特定神經元組成的細胞群,能調節體液。)
研究也發現,WNK1蛋白質的活化,會進一步促進細胞膜上「鉀離子通道Kv3.1」的功能,使OVLT神經元增加傳遞訊息到下游神經迴路,提高抗利尿激素的釋放,刺激腎臟再吸收水分,最後降低血液的滲透壓。
黃朝榮表示,過往認為位於室周器的神經元,它的細胞膜上有一種能夠感受膜張力變化的陽離子通道。但這個研究發現的滲透壓感測器WNK1蛋白質是位在細胞內,細胞外滲透壓上升時會增強活性,並活化細胞膜上的特定鉀離子通道Kv3.1,來增加OVLT神經細胞活性。
連正章特別指出,一般認為活化細胞膜上的鉀離子通道會抑制神經的活性,然而這次研究中的Kv3.1,是一旦活化後即快速關閉,不會一直抑制神經活性。
在連正章先前(2003年)的研究中,已利用電腦模擬及電生理學實驗的方式,證明Kv3.1通道有獨特的動力學特性,是促進神經活化較高頻率的關鍵。未來,連正章將探討WNK1活化Kv3.1通道的分子機制。
中研院分子生物研究所副研究員林書葦評論,這份研究的重要在於提出一個新穎的滲透壓偵測機制。
林書葦也指出當體內水分不足,大腦感受到滲透壓上升時,會一方面驅動飲水行為來補充水分,一方面促進抗利尿激素的釋放,以減少水分的流失。
不過這篇研究中,當小鼠被剔除WNK1基因,只會影響抗利尿激素的釋放,導致小鼠多尿、尿液的滲透壓降低,但不影響小鼠喝水的量。林書葦認為,這代表還有別的滲透壓感測器的存在,也暗示神經系統利用不同的滲透壓感測機制,來調控不同的行為和生理反應。
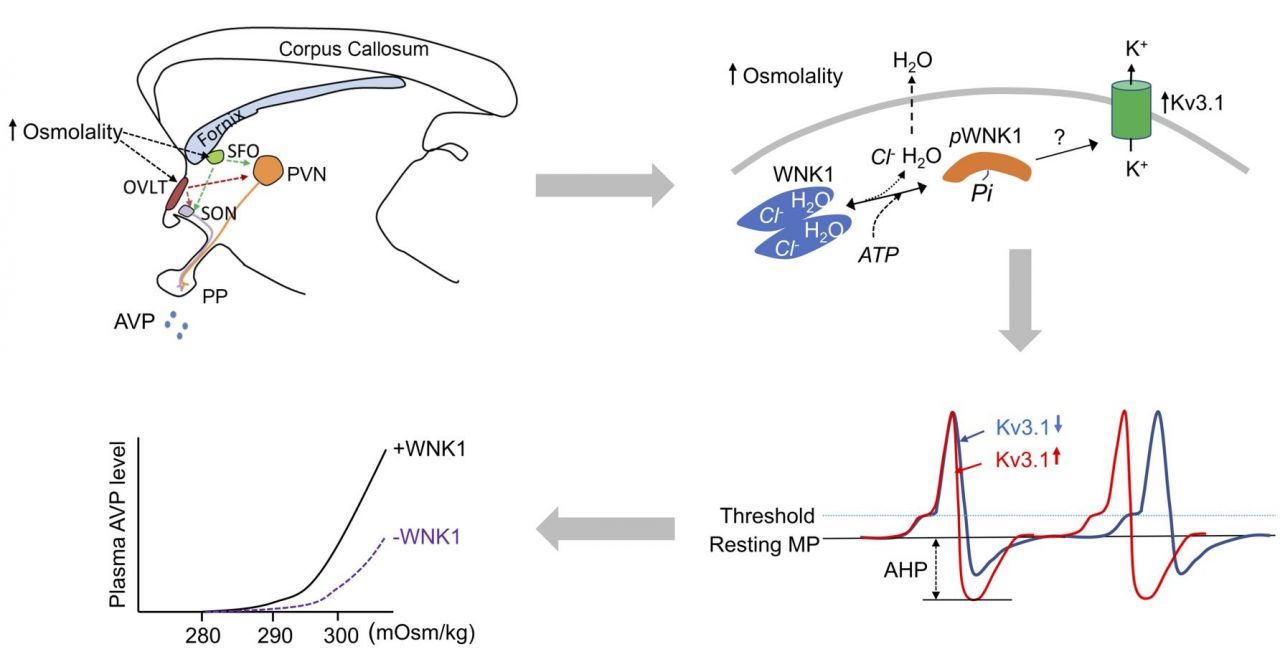
左上: 位於大腦第三腦室周圍的OVLT與SFO核區,可以感知滲透壓的上升而活化,進而活化下游的下視丘腦PVN與SON核區,並釋放抗利尿激素(AVP)。右上: OVLT神經元,表現一種叫做WNK1 的蛋白質,可以感知滲透壓的上升而活化(磷酸化),並進一步促進膜上鉀離子通道Kv3.1的功能。左下: 相對於沒有活化的WNK1 (-WNK1),活化後的WNK1 (+WNK),可以增加抗利尿激素的釋放。右下: OVLT神經元細胞膜上一群鉀離子通道Kv3.1的功能上升,神經衝動的頻率上升。反之,鉀離子通道Kv3.1的功能下降,神經衝動的頻率下降。
參考來源:https://smctw.tw/15639/
論文:https://www.jci.org/articles/view/164222
(報導/劉馨香)









