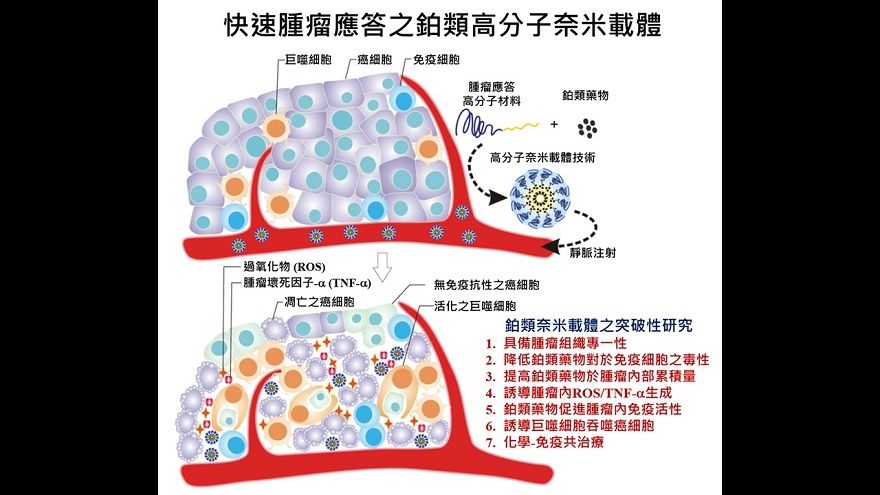
今(15)日,亞東醫院宣布放射部主任熊佩韋與國立陽明交通大學生物醫學工程研究所團隊攜手合作,耗時六年時間,開發出一種可以將鉑類抗癌藥物 (platinum-based drug)在腫瘤組織累積的奈米材料。研究也發現,此奈米材料可以達到腫瘤的免疫治療與化學治療雙重功效,同時大幅抑制腫瘤增生,降低腫瘤治療的副作用。研究結果已刊登在國際頂尖期刊《Biomaterials》當中。
熊佩韋表示,腫瘤組織是一個複雜的系統,其組成包含癌細胞、免疫細胞、纖維母細胞等。癌細胞會影響腫瘤組織中的各類細胞功能,並營造出適合癌細胞生長的環境。在此情況之下,化學治療的效果不僅可能降低,也可能造成腫瘤組織或自體免疫系統無法完全發揮對抗癌細胞生長的能力。
因此,熊佩韋與國立陽明交通大學團隊合作,開發出一種能將鉑類抗癌藥物累積到腫瘤組織的奈米材料。當奈米材料被腫瘤組織當中的癌細胞與巨噬細胞吞噬 (endo-/phagocytosis),便能快速釋放材料內部的鉑類抗癌藥物,在腫瘤處產生大量活性氧物質 (reactive oxygen species, ROS) 以直接毒殺癌細胞,並降低癌細胞的CD47抗原表現與重啟巨噬細胞的免疫抗癌能力 (antitumor immunity)。
熊佩韋表示,這樣的癌症治療方式相較於單一的藥物治療,能夠達成免疫治療 (immunotherapy) 與化學治療 (chemotherapy) 都無法達成的雙重治療效果。
熊佩韋補充,當癌細胞的CD47抗原過度表現時,免疫細胞就無法有效發揮功能,體內的巨噬細胞也會在腫瘤組織內被馴化成不具攻擊能力的細胞。因此,透過鉑類抗癌藥物釋放之後產生的活性氧,能夠達到刺激的作用,成功讓巨噬細胞轉化成可以辨識並殺死CD47抗原表現不足的癌細胞,達到腫瘤治療效果。
在本次的研究中,熊佩韋與國立陽明交通大學團隊也針對臺灣的國病之一—— 大腸直腸癌 (colon cancer) 進行動物實驗治療測試。研究發現,帶有大腸直腸癌的老鼠接受鉑類抗癌藥物之後,發現具有良好的抗癌效果。熊佩韋說,這次的研究不僅成功開發癌症奈米藥物,更是對未來的癌症治療趨勢提供的新的思考方向。
期刊原文連結: https://europepmc.org/article/med/34252800
(報導 / 吳培安)


- Global Bio and Investment Monthly
- 讀者服務電話:+886 2 2726 1065時間:週一 ~ 週五 09:00 ~ 18:00
- 服務信箱:[email protected]
- 地址:110臺北市信義區信義路六段29號2樓之一, Taiwan
- Copyright© 2024 環球生技多媒體股份有限公司. All rights reserved.本文內容受著作權法保護,如有引用請註明出處。授權申請。隱私宣告Privacy。會員條款User Terms。
為了提供您最佳的服務,本網站會在您的電腦中放置並取用我們的 Cookie,若您不願接受 Cookie 的寫入,您可在您使用的瀏覽器功能項中
設定隱私權等級為高,即可拒絕 Cookie 的寫入,但可能會導至網站某些功能無法正常執行 。