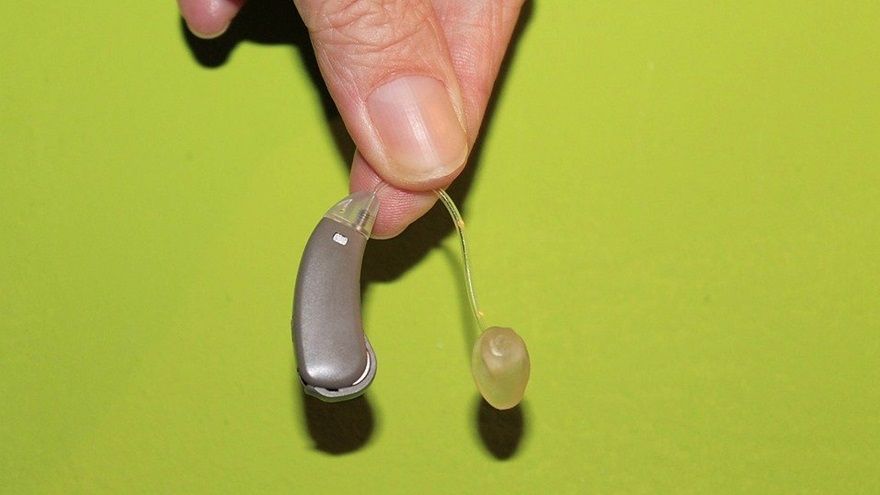
美國時間11日,博士音響(Bose)宣布,其已經取得美國FDA創新醫材認定(de novo clearance)認證的助聽器產品SoundControl,將在本月18日上市,供輕至中度聽力喪失的成人患者使用,且消費者可不需經醫師指示或處方簽,直接透過智慧型手機App調整設定,成為繼Apple公司在2018年推出感測心電圖的Apple watch後,另一電子消費產品巨頭跨入醫療器材的實例。
此產品的前一代助聽器版本,早先已在2018年10月獲得FDA的創新醫材認定(de novo clearance),其特色為直面消費者(direct-to-consumer),即不須醫師指示、消費者就可自行組裝的助聽器版本;上週,新的版本剛取得FDA的實質相等性認定,其外觀已調整成與傳統助聽器相似。
Bose表示,使用者也可以調整音量、音高和重低音(treble and bass)等,而無須進行處方籤或聽力測試,也可和Bose免費一對一尋求協助。此外,這項產品配備的聚焦功能,可讓使用者在不同模式間切換,例如:過濾嘈雜的空間雜音、專注於前方說話者的聲音,或是接收所有來自空間環境的聲音等。
Bose Hear品類經理(category director) Brian Maguire表示,光是在美國就有將近4800萬人因聽損損害生活品質,但治療方式的費用和複雜性,成為患者尋求協助的主要阻礙。
在美國,處方助聽器的費用可達數千美元,且很少由醫療保險業者全額支付;雖然商店能買到較便宜的個人擴音輔具(或稱輔聽器,personal sound amplification products),但在效能和可調整性上都不若助聽器,且未在FDA的監管範圍內。
雖然此產品還不屬於臨櫃(off-the-shelf)可取得的醫材,仍需從具專業執照的助聽器選配師取得。不過,此產品已成為FDA自2017年起,研擬有關臨櫃助聽器新法規的重要項目,此法規預計在未來推出。
Bose表示,這項產品預期價格為849.95美元(約2.38萬元台幣),預計在本月稍晚啟動首波銷售,範圍包括美國麻薩諸塞州、蒙大拿州、北卡羅來納州、南卡羅來納州、德州等。
目前依據聽力受損程度的不同,患者可使用助聽器,或是更進階的人工電子耳(人工耳蝸)作為聽覺輔具,能有效治療聽損的藥物非常少。
在國內的聽損領域中,陽明交通大學生物醫學工程學系助理教授賴穎暉,正透過陽明交大、中研院、振興醫院三方合作,開發AI降造聰明電子耳系統;馬偕醫學院生物醫學研究所許益超副教授團隊,也正研究透過基因療法或iPS細胞治療聽損的動物模型研究。
參考資料:
https://www.theverge.com/2021/5/11/22430485/bose-soundcontrol-hearing-aid-fda-cleared
(編譯 / 吳培安)
下一篇