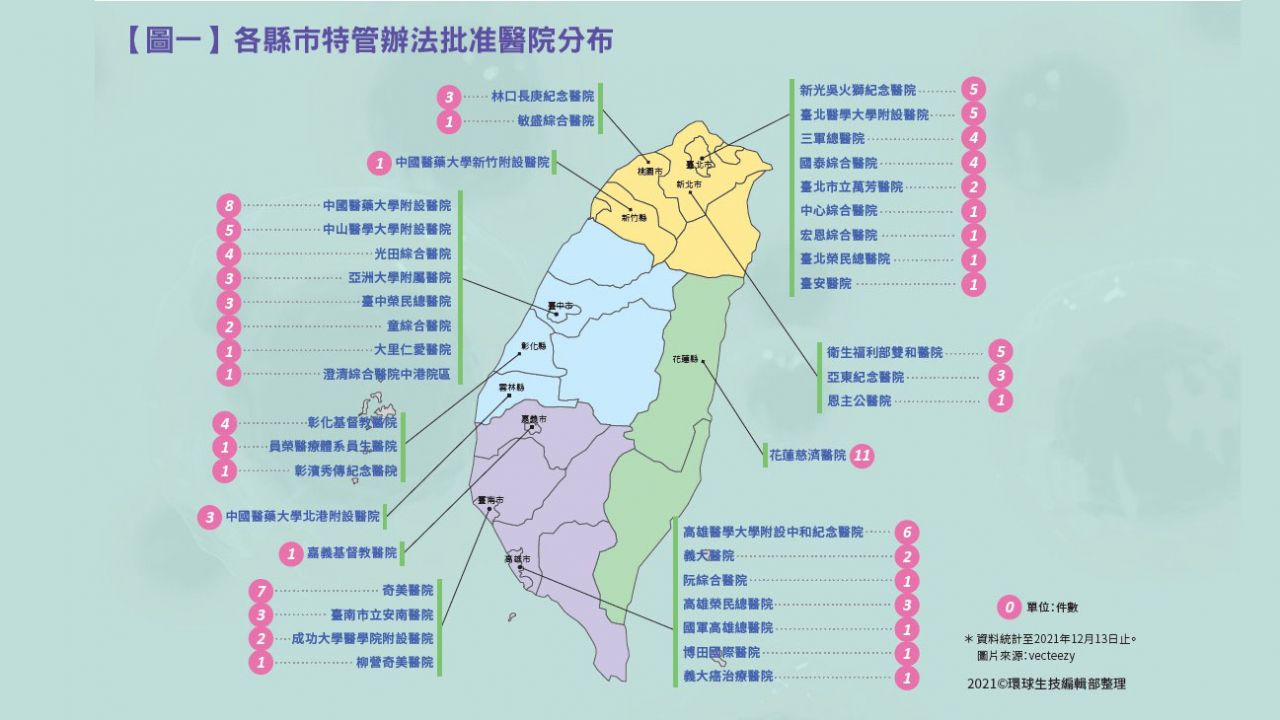
衛福部《特管辦法》上路三年多,迄今累積114件細胞治療案核可,全臺41家醫院、20家細胞製程業者熱烈響應,但民眾至今仍不清楚細胞治療成效究竟如何?衛福部常務次長石崇良表示,目前預計以退化性關節炎治療收案數據,與健康大數據資料庫進行真實世界研究,以提供具科學性的成效報告,但癌友最關切的癌症免疫細胞治療,仍需要更多的時間累積病例才能分析。
撰文/吳培安
衛生福利部《特定醫療技術檢查檢驗醫療儀器施行或使用管理辦法》(簡稱《特管辦法》)開放六大類自體細胞治療,透過醫院專科醫師和擁有優良組織規範認證(GTP)資格的細胞製備中心(cell processing unit, CPU)的業者合作,得以依據《特管辦法》附表三,提出六大類細胞治療項目施行計畫申請。
自2018年9月上路三年多,至2021年12月13日為止共累積至114件,全臺已經有41家醫院、20家細胞治療CPU業者成功取得核可;雖然衛福部尚未公布最新統計數字,但統計至2020年底、核准64件細胞治療計畫時,全臺總收案已達到307人。(圖一)
然而,這些療法,要價往往動輒數十萬元、完整療程甚至可達百萬元,但主管機關至今仍未公布各類型細胞治療的成效報告。如何以具體的療效追蹤數據說服民眾、把關醫療品質,成為政府推動創新再生醫療的重大挑戰。
對此,衛福部常務次長石崇良表示,衛福部正依據「特管辦法細胞治療技術銜接細胞製劑應檢附技術性資料指引」,透過國衛院群體健康科學研究所與業者合作,從政府跨部會建立的「健康大數據永續平台」中,篩選出足以作為對照的患者電子病歷,與細胞治療業者的真實世界數據(Real-World Data, RWD)做比對。
石崇良表示,「現在還需要一段時間追蹤。倘若這樣的嘗試成功,日後就能將具備科學性的統計報告提供給民眾參考,也有機會成為日後業者申請查驗登記時的參考資料,有望縮短上市時間。」
現任衛福部醫事司司長衛福部常務次長石崇良表示,期待在2022年就能通過「再生醫療三法」,建立全面性的法規環境。(攝影 / 吳培安)
特管辦法41家醫院
20家細胞製備業者熱烈響應
截至12月13日,全臺已有41家醫院、20家細胞治療CPU業者成功取得核可。
不過,如果不是同醫院、同CPU、同適應症的申請案,都必須重新申請,視為獨立的申請項目。(註:亦有醫院與自建CPU醫院
當前六大類細胞治療項目,依核可件數由多至少為:88件自體免疫細胞治療、9件自體軟骨細胞治療、7件自體骨髓間質幹細胞治療、7件脂肪幹細胞移植、3件自體纖維母細胞移植;至於CD34+篩選周邊血幹細胞,目前還沒有項目獲得核可。(表一)
而以適應症來看,114件細胞治療申請案之中,有88件都是針對癌症;17件是針對退化性關節炎及膝關節軟骨缺損,或僅針對膝關節軟骨缺損;4件是針對皮膚缺陷(皺紋、凹洞及疤痕填補修復、皮下及軟組織缺損);3件針對脊椎損傷,2件針對慢性或滿六週未癒合的困難傷口。
目前衛福部僅開放「自體」(Autologous)用途的細胞移植或治療,必須仰賴醫院專科醫師,由患者取出特定的細胞,經由CPU業者的細胞製備程序加以擴增,再透過輸注或手術送回患者體內。透過健康捐贈者提供細胞的「異體」(allogenic)細胞療法,目前仍不在《特管辦法》開放範圍內。
癌症免疫細胞治療最受業者期待
佔總件數超過75%
114件獲核可細胞治療計畫中,就有多達88件是癌症免疫細胞治療,顯見衛福部透過《特管辦法》開放細胞治療的重大期待之一,就是為治療選擇有限的癌症患者,提供新的治療選項,免疫細胞治療也可說是《特管辦法》中業者最躍躍欲試的開放項目。
88件之中,光是實體癌(solid tumor)治療就多達83件,其中65件是實體癌第四期、18件是經過標準治療無效的第一至第三期實體...