今年3月中,Orchard Therapeutics的罕見疾病——異染性腦白質退化症(MLD)基因療法Lenmeldy (atidarsagene autotemcel),獲得美國食品藥物管理局(FDA)批准,其高達425萬美元、相當於新臺幣1.36億元的驚人價格,也刷新美國「史上最貴藥物」的紀錄!
事實上,2024年1月全美最貴的10種藥物中,就有6種就屬於基因療法。由於具有一次性治癒的潛力,即使基因療法藥價高昂、或是可能產生不良反應,依然成為先天性遺傳疾病患者的希望。
什麼是基因療法?
根據FDA的定義,基因療法的目標是調整或操控基因,藉以改變活細胞的生物學性質。
最常見的兩種療法形式,其一是藉由病毒載體攜帶功能性基因片段、將其遞送到患者體內(in vivo)的目標組織細胞中,進而彌補或修正患者失去正常功能的基因,達成從讓患者不再需要長期服藥的功效。適應症多為先天性的罕見疾病。
其二是嵌合抗原受體T細胞(CAR-T)療法,藉由體外(ex vivo)基因工程修飾T細胞、增加其對特定標靶的靶向性後,再輸注到患者體內,不過FDA迄今批准的CAR-T療法都屬於自體CAR-T療法,必須先抽取出患者血液才能加工。目前獲批產品的適應症,都屬於血液惡性腫瘤,尚未有針對實體腫瘤的CAR-T產品。
動輒要價千萬元是常態!基因療法為何這麼貴?
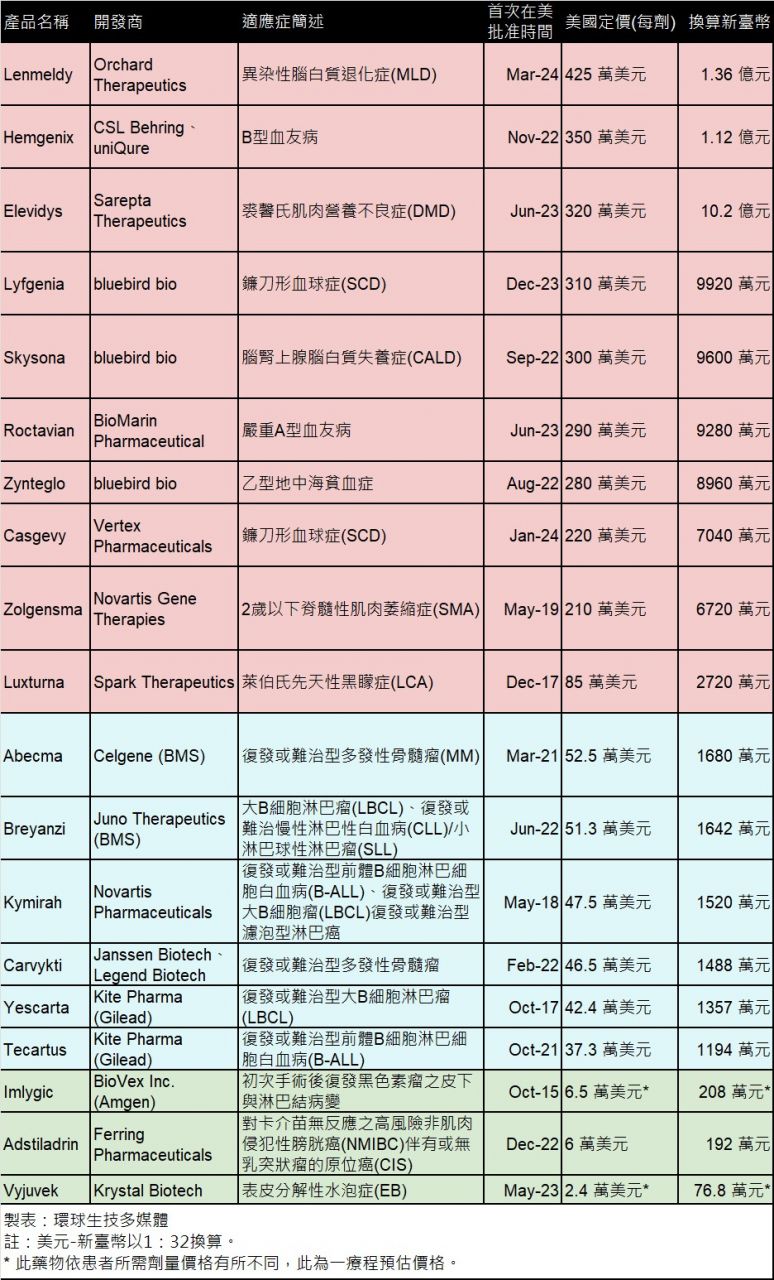
根據FDA網站及網路公開資訊,本刊彙整目前FDA批准的19項基因療法及在美國定價,如附表所示。其中排名前10名的高價位區段基因療法,雖然都主打只需一劑即可獲得終生療效,但每劑都要價新臺幣2千萬元以上,且價格最高的3項基因療法產品,換算新臺幣都超過1億元!
另一方面,FDA所批准的6項CAR-T療法產品,最高價者為每劑52.5萬美元(約新臺幣1,680萬元),最低價者也要37.3萬美元(約新臺幣1,194萬元);即使是較低價的基因療法,一個療程也需要約2.4萬美元(約新臺幣77萬元) ~6.5萬美元(約新臺幣208萬元)。
為什麼基因療法價格這麼貴?根據Chi Heem Wong等人2023年11月於學術期刊《Gene Therapy》刊登專文表示,箇中原因是基因療法相較於其他藥物領域,仍屬於剛起步階段,且製藥商在決定價格時,也考慮到潛在的臨床效益、開發成本、風險和不確定性。
臨床益處方面包括與傳統治療相比,基因療法能夠顯著延長壽命或緩解症狀,並解決罕見疾病治療中經常未被滿足的需求,因此在製藥商眼中屬於合理價格。
然而,這麼高的價格依然引起付款人(例如醫療保險業者)、患者、醫師及政策制定者的擔憂。新獲批上市的基因療法定價對大多數患者來說,都是難以自己負擔的天價,且不同的基因療法,獲得保險給付的範圍也不同。
以美國而言,許多健康保險並不給付已經獲批上市的基因療法,或是限制1年內可以接受特定療法治療的患者人數,導致出現即使患者有健康保險,但基因療法對他們來說依然是遙不可及的現象。
而在臺灣,雖然再生醫療專法目前尚在立法院審議中,但衛福部食藥署(TFDA)已經批准兩項基因療法產品,分別為諾華(Novartis)的Zolgensma基因療法,以及CAR-T療法Kymriah。
其中,一劑要價新臺幣4900萬元的Zolgensma,在去(2023)年8月起納入健保給付,成為國內首次將罕病基因療法納入健保給付的案例;Kymriah未納健保給付前的自費價格約為1200萬~1300萬元,但在2023年11月起開始有條件納入暫時性支付清單,降至一次治療819萬元,額度為終生一次。
雖然這兩項基因療法產品都順利納入健保,但無論未來再生醫療專法是否通過,基因療法都將推陳出新,期帶來的高價挑戰與健保系統韌性,都將成為臺灣面對未來新興醫療技術與產品,必須持續思考的問題。
延伸閱讀:2024年,健保多項政策革新將啟動,近年商業保險與創新醫療產品結合的喜訊頻傳。請見本刊Vol. 112期封面故事《未來醫療新「保」典!?》
基因療法藥價破紀錄 恐將成常態!
展望未來,雖然基因療法的開發依然存在諸多困難,但隨著技術日益成熟以及法規單位的支持,仍可預期未來基因療法上市的速度將出現加快趨勢。
在FDA目前批准的19項基因療法,在2021年前,幾乎是一年批准1或2項,但2022年就批准了6項,2023年批准4項,2024年第一季至今日已經批准2項產品。
近期FDA可能會陸續出爐批准結果的,還有Rocket Pharmaceuticals的免疫缺陷基因療法Kresladi、輝瑞的B型血友病基因療法Fidanacogene Elaparvovec、Abeona Therapeutics的泡泡龍基因療法Pz-cel等等。
未來高價基因療法不斷刷新藥價紀錄,可能將成常態。各國的因應方式,除了透過醫療科技評估(HTA)機制納入健康保險給付、或藉由基金會籌措醫療費用之外,也有透過國內自主開發產品或在地化生產,降低基因療法所需的費用。
據了解,雖然我國目前尚未有自主研發的基因療法候選產品,但也有6家生技業者投入CAR-T細胞療法開發,希望縮短細胞製程時間、或是採用非病毒式基因改造技術,包括:宇越生醫、沛爾生醫、承寶生技、創恩生醫、先驅生技、長聖生技;亦或是利用新型T細胞修飾技術開發產品,例如賽昂生醫的武裝型T細胞(armed T)。
延伸閱讀:盤點臺灣6家CAR-T細胞療法最新進展 臺、美臨床追趕國際!







