背景
近年來,國際政經局勢的變化促使全球製藥產業加速供應鏈重組。隨著醫藥技術的創新與突破,各國紛紛運用先進技術推動更具彈性與創新性的藥品生產模式,強化現有產品的製造能力,並積極推出新藥,以因應目前未被滿足的醫療需求。
先進製造(Advanced Manufacturing)是新型或創新應用的醫療產品製造技術的統稱,這些技術可以提高藥品品質、解決藥品短缺問題並加快上市時間。包含連續製造(Continuous Manufacturing)、分散式製造(Distributed Manufacturing, DM)、3D列印(three-dimensional printing)以及人工智慧(Artificial Intelligence, AI)等,整合新穎的技術方法,或以創新方式使用現有的技術,或應用尚未定義的新生產方法,或將過去經驗應用於新的不同的領域中。
美國FDA於2025年1月2日推出「先進製造技術認定計畫指引」(Advanced Manufacturing Technologies Designation Program Guidance for Industry)的最終版,鼓勵儘早採用先進製造技術(Advanced Manufacturing Technologies, AMTs),期望透過提高製造效率和供應的穩定性,使病人受益。
先進製造技術認定計畫指引重點:
該指引說明,一項新技術尚未在先前藥品核准申請中使用過,即符合AMT,當認定的AMT已應用於多個已核准的監管產品中,FDA可能會不再將此AMT列入早期溝通評估。
而個人或公司所開發的新技術皆可向FDA提出該技術的AMT認定申請,欲申請認定的AMT必須證明此AMT與現有製造方法相比具有同等或更好的藥物品質,獲得FDA先進製造技術AMT認定的則為AMT認定持有者。AMT認定持有者亦可將AMT技術授權給藥證申請人,以在NDA、ANDA、BLA或IND申請時引用AMT資訊。
獲得AMT認定將有機會提早與監管單位溝通,包含了藥品製造領導專家與FDA高階管理人員和其他經驗豐富的FDA工作人員組成的團隊,將一同參與AMT的協作、跨學科審查。溝通內容如AMT設計或開發問題、認定AMT相關的提交資料等,皆可與FDA品質評估團隊進行協調,溝通結果也將做為未來開發商或製造商藥證申請時化學、製造與管制(Chemistry, Manufacturing, and Controls, CMC)的評估依據,以加速藥品上市時間。
Cellares獲得首個FDA的AMT認定
Cellares是一家專業的臨床和細胞療法製造商業化的綜合開發和製造組織(Integrated Development and Manufacturing Organization, IDMO),其Cell Shuttle於2025年4月1日獲得FDA CBER的先進製造技術AMT認定,可用於自動化細胞療法的生產,以提高細胞療法的效率、品質和可擴展性。Cellares的自動化細胞治療生產平台Cell Shuttle已於2024年3月通過cGMP標準,其佔地面積僅相當於一輛卡車,並結合了在一台設備中完成整個細胞療法生產運作所需的所有技術。Cell Shuttle實現了自動化、端到端end-to-end的細胞療法製造,包括細胞純化收集、細胞選擇、傳遞、轉染、活化、擴增和配製過程,同時符合細胞療法商業化最終產品的規格。該系統具有可靠且能大規模生產高品質治療產品的能力,可提供給小型早期生物技術公司和商業化細胞療法的大型製藥公司,擴展且經濟高效益的細胞療法製造,具有改變病人治療結果的潛力。
必治妥施貴寶BMS已與Cellares達成了3.8 億美元的協議,預留了CAR-T療法Breyanzi和Abecma以及未來細胞療法候選藥物的產能。另外Kite Pharma與Cellares合作對Cell Shuttle進行了概念驗證評估,以加強Kite Pharma對CAR-T細胞療法的製造能力。
利用Cellares Cell Shuttle平台製造服務的藥商將可能優先獲得FDA的快速審查,更有效率的符合監管標準,縮短IND和BLA的時間,加速藥品上市。
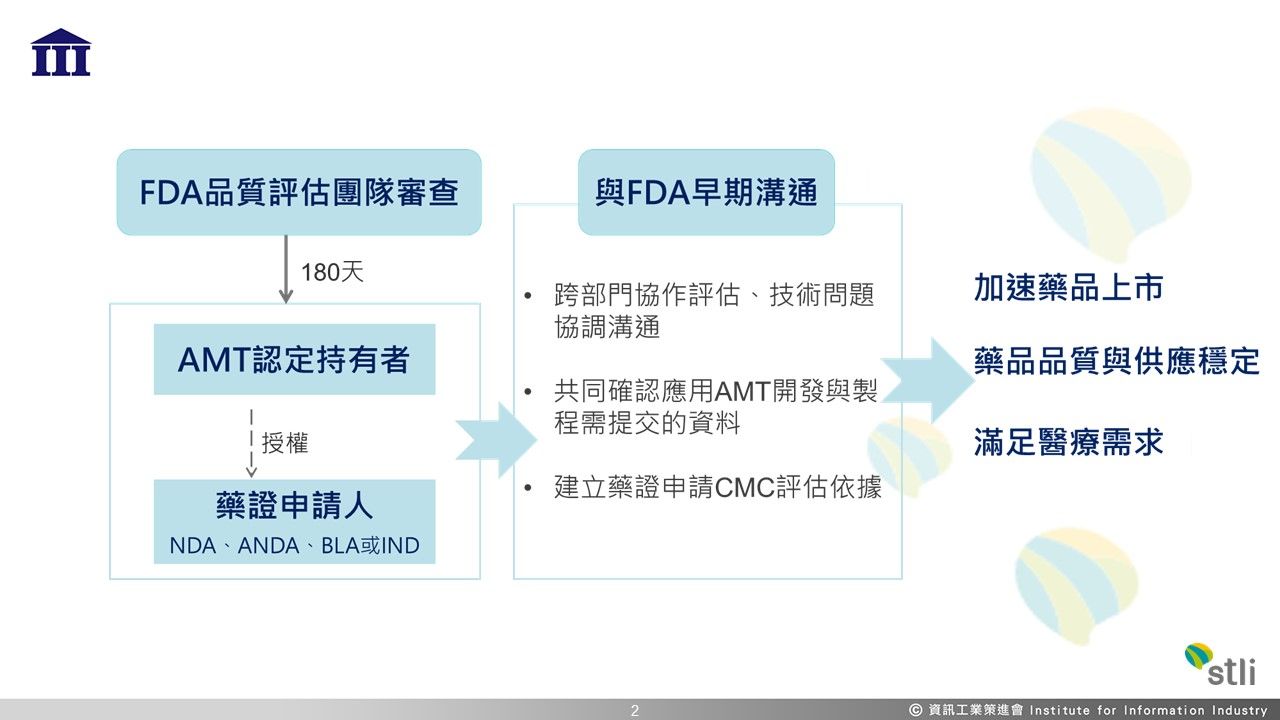 美國先進製造技術認定對藥廠的優勢 (資料來源:資策會科法所繪製)
美國先進製造技術認定對藥廠的優勢 (資料來源:資策會科法所繪製)
撰文/資策會科技法律研究所 陳怡錦 法律研究員









