CGT法規監管挑戰複雜!專家建議:與法規監管單位對話越早越好!
2025-12-16 / 記者 彭梓涵
由經濟部產業技術司指導、資策會科技法律研究所主辦的「國際法規線上論壇」,聚焦於細胞與基因治療(CGT)的法規監管挑戰、現況與最新發展,分別於9月26日、10月29日舉辦兩場活動,邀請到AlanLiss、IraKrefting兩位曾任職美國FDA的法規監管專家,以及SparkTherapeutics前法規與政策內容管理主管、現任BIO科學法規事務副總裁SnehalNaik,透過專題演講、綜合討論,為...
東協區域聯合評估機制助降低藥品跨國上市重複審查成本及時間
2025-12-02 / 資策會科法所
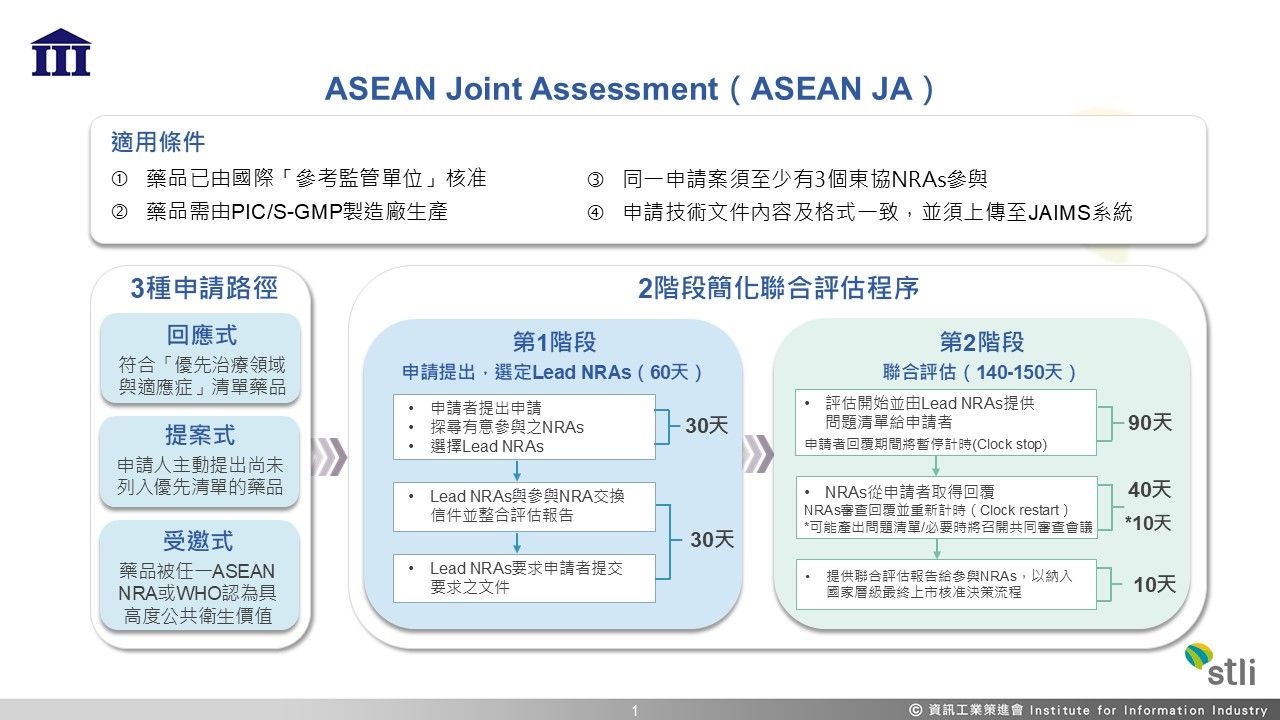
製藥公司在拓展海外市場往往面臨各國單獨審查、資源分散、上市申請審查時間冗長等挑戰,可能導致錯過搶占市場之先機。東協聯合評估(ASEANJointAssessment,ASEANJA)接受同一藥品可同時提交至少3個參與東協會員國藥品監管單位(NationalRegulatoryAuthorities,NRAs)之上市審查申請,由各NRAs國聯合評估並產出聯合評估報告,再由各國監管單位依該國程序做出最...
生技醫藥產業淨零轉型策略出爐!專家提倡差異化目標與策略 促進跨界合作
2025-11-29 / 新聞中心
作者:資誠聯合會計師事務所生醫產業服務團隊在經濟部產業技術司指導下、資策會科法所主辦,資誠聯合會計師事務所執行兩場專家閉門會議,主題分別為「國際生技醫藥淨零永續發展趨勢與台灣發展建議」、以及「台灣生技醫藥淨零永續制度發展方向與考量」,於2025年9月至10月進行。會議中邀請到生技製藥、醫療器材、再生醫療與醫藥物流業者,以及學研機構專家共同討論台灣生技醫藥產業在推動淨零永續過程的經驗與面臨的挑戰。 ...
生技醫藥淨零轉型面臨獨特挑戰:法規和確效為變革挑戰 業者籲政府制定差異化制度
2025-11-29 / 新聞中心
作者:資誠聯合會計師事務所生醫產業服務團隊在經濟部產業技術司指導下、資策會科法所主辦,資誠聯合會計師事務所執行兩場專家閉門會議,主題分別為「國際生技醫藥淨零永續發展趨勢與台灣發展建議」、以及「台灣生技醫藥淨零永續制度發展方向與考量」,於2025年9月至10月進行。會議中邀請到生技製藥、醫療器材、再生醫療與醫藥物流業者,以及學研機構專家共同討論台灣生技醫藥產業在推動淨零永續過程的經驗與面臨的挑戰。 ...
CGT法規監管變動快!專家:與監管機構早期溝通至關重要
2025-11-06 / 記者 吳培安
10月29日,由經濟部產業技術司指導、資策會科技法律研究所主辦的「國際法規線上論壇:美國細胞與基因治療(CGT)產品的法規框架—現況與新發展」,第二場邀請到SparkTherapeutics前法規與政策內容管理主管、現任生物創新組織(BIO)科學法規事務副總裁SnehalNaik,並於綜合討論中,與擁有豐富藥物法規策略與臨床經驗的洪筱玲博士對談,分析當前美國CGT監管動態,也提醒台灣...
專利制度對於創新與藥價可近性的兩難 資策會科法所匯聚法學專家 傳授風險控管心法
2025-10-22 / 記者 彭梓涵
2025年10月15日,由經濟部產業技術司指導、資策會科技法律研究所舉辦的「2025癌症健康治理及專利實務工作坊」,第二場「國際關鍵疾病藥物專利實務」場次,邀請台大法律學院李素華教授、萬國法律事務所呂紹凡律師、寰瀛法律事務所蘇佑倫律師、理律法律事務所黃裕煦專利師與北美智權集團劉家豪專利師、資策會科法所張羽筑副研究員,從法律、政策與產業實務三面向,共探專利制度如何支撐新藥研發、確保創新與藥價可近性的...
專家解析Biobank、健保資料庫資料治理挑戰、加速整合之道
2025-10-22 / 記者 吳培安
2025年10月15日,由經濟部產業技術司指導、資策會科技法律研究所舉辦的「2025癌症健康資料治理及專利實務工作坊」,在第一場「關鍵疾病健康資料治理」議題中,邀請中研院歐美研究所何之行博士、台灣人體生物資料庫(TaiwanBiobank)蘇明威資訊長,分享生物資料庫法制規範、治理與健康資料應用,更邀請曾主筆111年憲判字第13號「健保資料庫案」的前司法院大法官黃虹霞律師,與資策會科技法律研究所...
日本續推生物相似藥國產化政策 厚勞省再編5.7億日圓補助製造設施
2025-10-21 / 記者 彭梓涵
作者/資策會科技法律研究所跨域整合中心生醫衛政組黃毓瑩組長責任編輯:彭梓涵 日前國內生物相似藥開發業者重訊宣布,其開發的生物相似藥產品在臨床三期試驗豁免會議上獲得歐美監管單位支持,顯示歐美對該領域臨床評估的態度出現更具彈性的轉變。隨著各國積極推動生物相似藥發展,近日,日本厚生勞動省(MHLW)於10月12日發布《2026年度預算要求摘要》,在延續2024年編列65億日圓推動日本生物相似藥製造設施建...