FDA通過首個可調式人工水晶體系統
2017-11-23 / 記者 徐淨
美國食品藥物管理局(FDA)昨(22)日批准了RxSight的光調節水晶體(lightadjustablelens)和光傳遞設備(lightdeliverydevice,LDD),這是第一個可以在白內障手術後,對人工水晶體(intraocularlens,IOL)進行小幅度調整的醫療器械系統,幫助患者不戴眼鏡也能擁有良好視力。白內障通常是由於年紀增長,水晶體變硬或混濁,影響患者視力。也有些是由於外...
精準殺手?AI智慧型武器
2017-11-23 / 記者 趙育麟
據外電報導,近日於瑞士日內瓦召開的一場聯合國「特定常規武器公約」會議(ConventiononConventionalWeapons,CCW)播放了一段視頻,內容顯示裝備了人工智慧的微型無人機具有多麼可怕的威力。這些如同蜜蜂一般的空中殺人武器,可以自主決定攻擊對象。該視頻由著名的物理學家StephenHawking和美國新型產業大亨ElonMusk等人聯盟支持的「生命未來研究所」(Futureof...
三星Bioepis領先群雄 兩年四款生物相似藥獲批
2017-11-23 / 記者 李虎門
近日,三星另一藥廠Bioepis的生物相似性藥Ontruzant,獲得歐洲醫藥品管理局(EMEA)上市許可,也是歐盟批准第一個人類單株抗體(Trastuzumab)的生物相似藥。三星Bioepis的生物相似性藥,主要用於治療早期乳癌、轉移性乳癌,以及轉移性胃癌,其原廠參考藥物為羅氏藥廠Herceptin,也是羅氏銷售第二大的藥物,去年的銷售額就達67.8億美元,三星Bioepis社長高韓勝表示,「...
ViiV愛滋新藥獲准 FDA︰可減少對患者的毒性
2017-11-22 / 記者 李虎門
今日,美國食品藥物管理局(FDA)宣佈,批准ViiVHealthcare用於治療HIV-1(HumanImmunodeficiencyVirus)的新藥(Juluca)許可。特別的是,目前HIV治療方案中,均含有3種或更多的藥物聯合使用,而Juluca只含有兩種藥物來治療HIV患者。HIV是人類免疫缺乏病毒,俗稱愛滋病毒。根據美國疾病控制與預防中心(CentersforDiseaseControl...
14億美元!Zymeworks和Janssen衝刺雙特異性抗體技術
2017-11-22 / 記者 徐淨
Zymeworks(NYSE/TSX:ZYME)於本(11)月宣布,已和嬌生公司楊森藥廠(JanssenBiotech)簽署了授權協議,Zymeworks將其Azymetric™和EFECT™平臺授權予楊森,用於開發6種雙特異性抗體計畫(BispecificantibodyTherapeutics),並將高達14.5億美元的合約金用於推進其抗體藥物ZW25的臨床推進。Zym...
Patisiran獲FDA突破性療法認可
2017-11-21 / 記者 徐淨
AlnylamPharmaceuticals今(21)日宣布,美國食品藥物管理局(FDA)認可其RNAi藥物Patisiran為突破性療法,將有效加速其上市。該藥物為針對甲狀腺素運載蛋白(Transthyretin,TTR)發生基因突變所引起的遺傳性澱粉樣多發性神經病變(hereditarytransthyretin-mediatedATTRamyloidosis,hATTRamyloidosis...
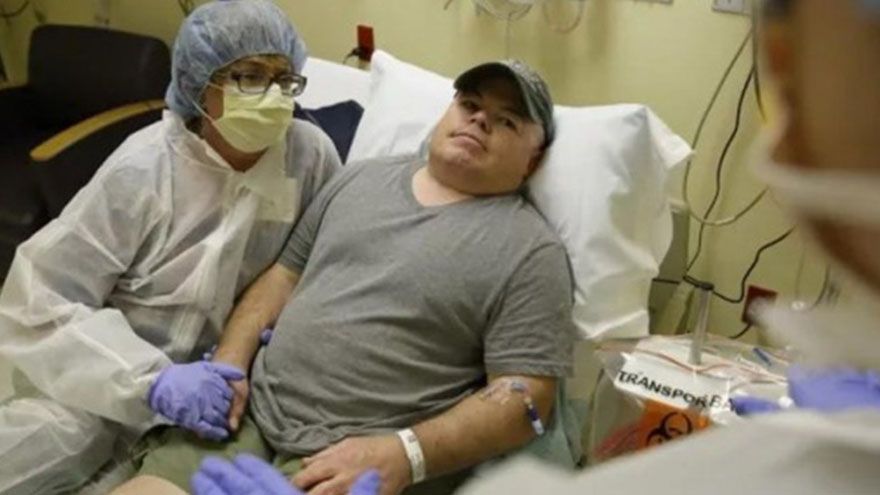
首次人體內基因編輯治療 有望治療罕病雷氏症候群
2017-11-21 / 記者 林以璿
本(11)月,人類首例體內基因編輯治療在美國展開。44歲的美國男子BrianMadeux在加州大學舊金山分校貝尼奧夫兒童醫院,接受了這項實驗性治療,希望可以治癒罕見遺傳性疾病雷氏症候群(RamsayHuntsyndrome)。雷氏症候群是一種罕見遺傳病。發病者主要是男性,症狀是缺少IDS基因,進而導致細胞累積有毒的代謝物。這些代謝物堆得越來越多,給患者的器官帶來傷害。此次治療所使用的基因編輯工具是...
默沙東投資Quartet灰臉收場
2017-11-21 / 記者 趙育麟
據外電報導,專注慢性神經疼痛新藥開發的生物技術公司四方醫藥(QuartetMedicine,以下簡稱四方),近來傳出將停止營運。這個由知名創投家,風險投資公司阿特拉斯(Atlas)基金大咖BruceBooth親自任職董事長的公司,在一年前還備受追捧、春風得意。如今,其治療慢性神經痛的止痛新藥GLP,在28天用藥的毒理學試驗中,最後幾天出現「預料之外」的神經學反應,這樣的結果讓公司正逐步停止營運。在...
輝瑞十年磨一劍 首款腎細胞癌輔助療法獲批
2017-11-20 / 記者 李虎門
近日,輝瑞(Pfizer)宣佈,美國食品藥物管理局(FDA)批准了旗下SUTENT®(SunitinibMalate),其用於輔助治療腎臟移除後,腎癌(腎細胞癌)復發高危險群的成人患者。全世界每年約有30.4萬例新診斷的腎癌病例,約占所有癌症的2-3%。而腎細胞癌(RCC)是腎癌中最常見的類型,約占90%左右。大約75%的患者被診斷為非轉移性透明細胞後,其中70-80%的患者將接受腎切除術...
FDA批准 首個癌症基因檢測平台
2017-11-19 / 記者 趙育麟
美國食品與藥品監督管理局(FDA)日前宣布,批准基於次世代定序技術(NGS)的癌症基因檢測分析平台MSK-IMPACT™,這是NGS首個經FDA批准用於癌症基因檢測的panel。MSK-IMPACT™是一個更加靈活、全面的癌症基因檢測平台,由紀念斯隆·凱特琳癌症研究中心(MemorialSloanKetteringCancerCenter,MSK)病理科開發。...
不止做鏡頭 Nikon代理再生醫療新藥進三期臨床
2017-11-18 / 記者 林以璿
Nikon近日宣布,其代理的Athersys公司幹細胞藥物MultiStem,將進入三期臨床試驗,有望成為治療急性腦梗塞的再生醫療新療法,預計2019年可以註冊新藥。隨著人口的老齡化,腦梗塞是常見的心腦血管疾病。而再生醫療是日本的重要產業,再生醫療的突破性新產品,將可以獲得優先審評和快速通道的資格。看準商機,2015年以來,Nikon就開始悄悄地向健康領域轉移,與瑞士細胞生產代工廠龍沙(Lonza...
默沙東投資3.74 億 合作免疫療法開發
2017-11-17 / 記者 李虎門
今日,腫瘤免疫治療公司CueBiopharma與默沙東(MSD)共同宣佈,達成研發合作和授權協議。根據這項協定,CueBiopharma將利用該公司的CUEBiologics技術平臺為默沙東開發能夠調節與自身免疫疾病相關的特定T淋巴細胞活性的生物製劑。而CueBiopharma會從默沙東獲得前期投資,且研發和上市過程中的里程金總計,可高達3.74億美元。無論是免疫檢查點抑制劑還是CAR-T療法,如...