俄羅斯斥資17億美金 以基因編輯培育新品種動植物
2019-05-30 / 記者 李林璦
近日,俄羅斯宣佈將進行一項斥資1110億盧布(約17億美元)的聯邦計畫,將支持該國研究人員發展以基因編輯技術培育新品種動植物的研究。據《Nature》報導,該計畫預計至2020年將培育10種基因編輯動植物新品種,至2027年將再培育另外20個新品種。該計畫將大麥、甜菜、小麥和馬鈴薯這4種農作物列為優先。根據聯合國糧食及農業組織的數據顯示,俄羅斯是世界上最大的大麥生產國,也是其他3種作物的主要生產國...
Amprion早期偵測帕金森氏症技術 獲FDA突破性醫材認可
2019-05-30 / 記者 彭梓涵
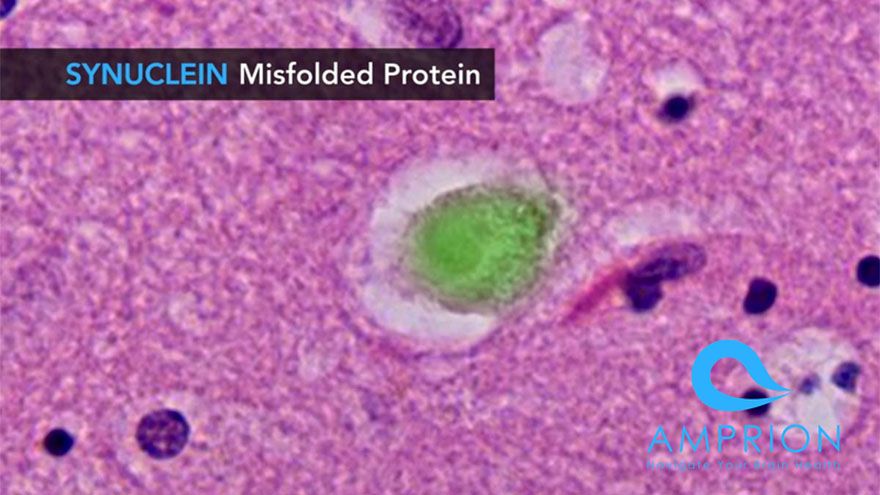
日前(28),Amprion公司宣布,其獨有蛋白質錯誤摺疊循環擴增(PMCA)技術,比目前現有的診斷方法,可偵測到更早階段的帕金森氏症疾病病程,因而獲得美國食品藥物管理局(FDA)突破性醫療器材認可。Amprion表示,若PMCA技術獲得FDA批准,Amprion預計將在未來18個月內推出PMCA測試市場,作為帕金森氏症的早期檢測工具。Amprion開發的PMCA技術,可在臨床症狀發作前,透過檢測...
拜耳淋巴癌療法獲FDA突破性治療核准 有望解決癌症復發難題
2019-05-30 / 記者 吳培安
今(美國時間29),德國拜耳(Bayer)宣布其藥物Aliqopa(copanlisib)獲得美國FDA突破性治療(BreakthroughTherapyDesignation)認證。此療法適用於復發性的邊緣區型淋巴癌(MZL)、過去接受過至少兩種全身療法的成人患者,有望解決MZL復發後化療/免疫療法效果不彰的醫療需求。此次FDA核准是根據關鍵臨床二期試驗CHRONOS-1研究的結果。在此研究中,...
Celgene免疫調節劑Revlimid獲FDA批准用於NHL首次無化療合併療法
2019-05-30 / 記者 薛瀹熢
美國時間28日,美國食品與藥物管理局(FDA)宣布批准製藥公司Celgene旗下Revlimid(lenalidomide)合併rituximab用於已接受過治療的濾泡淋巴瘤(FL)或邊緣區淋巴瘤(MZL)的成人治療。這也是FDA首次批准此類非霍奇金氏淋巴瘤(NHL)的無化療合併療法。Revlimid-rituximab合併療法的批准主要基於臨床三期試驗AUGMENT的資料。接受Revlimid-...
2019亞洲國際營養保健食品展 提供亞洲買家一站式媒合
2019-05-29 / 記者 彭梓涵
2019亞洲國際營養保健食品展(VitafoodsAsia)將在2019年9月25日至26日於新加坡再度亮相,展覽彙集科學、商業和政府機構的研發與創新。預計今年將來自超過60個國家6,000名參觀訪客與350多家參展商出席亞洲國際營養保健食品展,將為產業發展帶來更多機遇。新興品牌區匯聚了首次參展的創業團體和初創公司;國際展區展示來自澳洲、加拿大、法國、德國、日本、台灣及美國等多個國家和地區最新的營...
FDA核准AngioDynamics微創醫材臨床試驗申請 可望降低攝護腺癌治療影響
2019-05-29 / 記者 吳培安
今(美國時間28),美國FDA核准醫材公司AngioDynamics的NanoKnife的臨床先導性試驗(Pilotstudy),用以攝護腺癌腫瘤燒灼治療。若試驗順利完成,這項微創手術醫材將能提供局部攝護腺癌患者更為精準的替代方案,而不須接受整個腺體的治療。這項先導性試驗將在美國3個不同地點進行,共計6名患者參與,研究結果會成為AngioDynamics與FDA後續溝通的對話基礎。若後續順利取得核...
Allergan廣效躁鬱症藥物Vraylar獲FDA核准
2019-05-29 / 記者 薛瀹熢
美國時間28日,美國食品與藥物管理局(FDA)宣布核准了愛爾蘭製藥公司Allergan旗下躁鬱症藥物Vraylar(cariprazine)的補充新藥申請(sNDA),用於治療成人躁鬱症(bipolarIdisorder)相關的憂鬱症狀。Vraylar由匈牙利製藥公司GedeonRichter開發並授權給Allergan。該藥物在美國也被批准用於治療成人躁鬱症相關的狂躁症狀(manic)或混合型症...
禮來以近10億美元與Centrexion合作 拓展非鴉片類止痛藥物市場
2019-05-29 / 記者 彭梓涵
昨(28)日,禮來(EliLilly)宣布與CentrexionTherapeutics達成協議,禮來將支付Centrexion4750萬美元預付款,與5.75億美元開發和監管里程金,並獲得非鴉片類藥物CNTX-0290治療慢性疼痛的全球獨家權利。根據協議,若藥物進入市場Centrexion還將獲得3.75億美元(總交易金額共計近10億美元),雖然禮來獲得CNTX-0290的全球獨家權利,但藥物上...
香港交易所生物科技週開跑 8家新藥研發公司備受矚目
2019-05-28 / 記者 吳培安
今(28)起,香港交易所將在香港金融大會堂舉辦為期3日的2019生物科技週(HKEXBIOTECHWEEK2019),據外媒報導,目前有11間生物醫藥公司提交IPO上市申請,其中有8間為新成立的新藥研發公司,6間以癌症新藥研發為目標。 香港交易所自一年前實施上市新政以來,目前已成為全球第二大生物科技上市中心,聚集了為數眾多的專業投資人、分析師及顧問,是生技及醫療保健領域新創公司招募投資的重要場域。...
FDA前任局長Scott Gottlieb宣布重回NEA生命科學創投
2019-05-28 / 記者 薛瀹熢
近日,據《fiercebiotech》的資訊,FDA前任局長ScottGottlieb在辭去FDA的工作一個多月後,迅速宣布將回到他從前曾經任職過的生命科學風險投資公司(NewEnterpriseAssociates,NEA),成為該公司的特別合夥人。在進入政府工作之前,ScottGottlieb曾經在NEA任職十年。作為FDA最受歡迎的局長之一,過去他曾大力推行開放政策以緩解困難的藥物開發通道,...
Hologic、Cepheid、Roche性傳染病診斷獲FDA認可 補足公共衛生缺口
2019-05-28 / 記者 吳培安
近(24)日,美國食品藥物管理局(FDA)核准兩項分別檢測衣原體(chlaymydia)和淋病(gonorrhea)等性傳染病的檢驗設備,分別是Hologic子公司Gen-Probe的AptimaCombo2Assay和Cepheid的XpertCT/NG。它們是首批FDA核准用於喉嚨、直腸等生殖器以外區域的診斷設備,在過去僅用於尿液、陰道和子宮頸內膜的檢查。FDA在審核這兩項醫材時,參考了美國國...
川普本週將發布重大醫療政策 強制揭露藥物定價
2019-05-27 / 記者 吳培安
日(美國時間24)前,據《華爾街日報》報導,美國總統川普將在本週發布行政命令,要求美國醫療健康行業必須揭露處方藥定價,這項命令將造成對行業造成重大的影響。定價揭露是當前美國持續努力方向的目標之一。在美國,藥價不僅是由藥廠和醫療體系決定,醫療保險公司也在其中扮演重要的協商角色。據《華爾街日報》表示,有一未具名消息來源指出川普政府將利用聯邦政府的權力,強制將價格揭露當成降低醫療保險費用策略的一部分。然...