仁新黃先龍:仿效美國FDA加速、有條件批准 促進臺灣罕病藥物發展
2021-03-18 / 記者 彭梓涵
仁新醫藥(6696)為一家專注於開發創新藥物,以治療未被滿足醫療需求的疾病的新藥研發公司。由子公司BeliteBio™所開發的LBS-008已完成臨床1期,試驗數據顯示其可有效抑制RBP4且安全性極高。 目前也取得澳洲藥物管理局(TGA)的臨床試驗通知確認函(CTNacknowledgment),獲批准針對12-18歲的斯特格病變青少年病患進行臨床1b/2期試驗,預計將於今年啟動斯特格...
台灣20家孤兒藥廠類股新尖兵 瞄準罕藥藍海
2021-03-16 / 記者 彭梓涵
受益美國FDA的藥物評估與研究中心(CDER),2020年孤兒藥獲批創10年新高,擁有孤兒藥資格的新興療法獲批的數目達32個,更佔2020年獲批新藥的60.4%。國際罕病日(每年二月最後一天)甫過,再度掀起全球對罕藥開發的關注。台灣孤兒藥產業也已經成長至超過20家藥廠,異軍突起成為生技醫藥類股一支新尖兵,更不乏登上百元股價俱樂部者。如仁新、藥華藥、生華科、共信醫藥。近10年來,得益於FDA持續頒發...
晚期子宮頸癌數據積極! 賽諾菲/再生元免疫療法Libtayo提早結束3期試驗
2021-03-16 / 記者 彭梓涵
美國時間15日,賽諾菲(Sanofi)與再生元(Regeneron)宣布,其開發的免疫療法Libtayo治療晚期子宮頸癌的3期試驗,因為臨床結果數據積極,獨立數據監控委員會(IDMC)一致建議提早終止該試驗,Sanofi與Regeneron也將於今年提交數據給監管機構。 此為目前最大規模的晚期子宮頸癌3期臨床試驗,主要招募608名患有鱗狀細胞癌或腺癌的女性,患者會隨機分配至Libtayo單藥或常用...
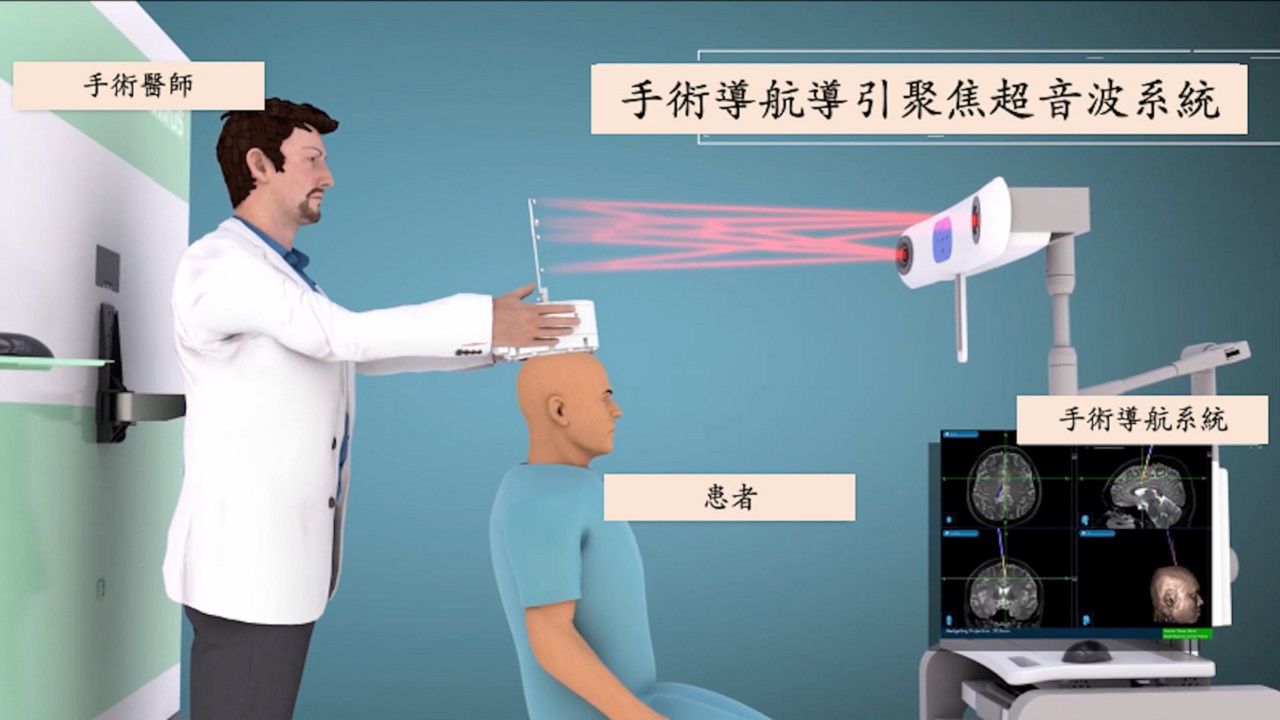
長庚首創手術導航聚焦超音波系統 完成6例惡性腦瘤臨床試驗 登《Science》子刊
2021-03-12 / 記者 彭梓涵
昨(11)日,長庚研究團隊表示,與國家衛生研究院及科技部合作開發之「手術導航導引聚焦超音波系統」,完成6例惡性腦瘤患者人體臨床試驗,分析其試驗結果顯示,聚焦超音波焦點定位,使手術精準度誤差範圍低於2公厘,以核磁共振檢查,血腦障壁也順利依時啟閉且無腦出血等不良副作用。 由於該技術獨創性與高度臨床應用價值已獲得世界多國專利,除了獲得國家新創獎及科技部最佳技轉獎(該技術已由浩宇生醫承接),亦被美國超音波...
國際生醫加速器 正從矽谷往全球各地發散
2021-03-11 / 記者 彭梓涵
2017~2019年間,全球創新經濟體總計創造了3兆美元產值,與全球7大工業國(G7)經濟體的國內生產總值(GDP)相當,創新創業生態圈正在從矽谷「全球化發展」,現今遍佈全球至少28個國家,總計約80個區域形成生態系、全球也成立了約3,000多個加速器。撰文/彭梓涵加速器(Accelerators)的概念源自2005年矽谷(SiliconValley)創業教父PaulGraham創辦的YCombi...
DCB數位健康國際加速器 4年完成37家公司輔導
2021-03-11 / 記者 彭梓涵
撰文/彭梓涵 攝影/吳培安2018年,財團法人生物技術開發中心(DCB)為迎接全球快速發展的數位健康產業(DigitalHealth),並促進推動臺灣生物醫學創新公司成長,成立了臺灣首個數位健康國際加速器—臺灣鳳凰計劃(TaiwanDigitalHealthAccelerator)。並同時與美國波士頓加速器MassChallenge合作,不僅聚焦數位健康,加上DCB數十年在生物醫藥累積...
南科管理局結盟上傑洋、金屬中心 共建TransMedx
2021-03-11 / 記者 彭梓涵
撰文/彭梓涵 攝影/吳培安臺灣全民健保、醫療水準舉世聞名,更是半導體、光電、精密機械研發生產的重鎮,科技部南部科學園區管理局(以下簡稱南科管理局)看好臺灣數位醫療,有潛力扮演國際重要角色,於2019年與金屬工業發展中心、及在輔導生醫新創團隊於國內外頗富盛名的上傑洋公司團隊,成立國內以創投角度經營,唯一專注醫材領域的加速器—南科新創醫療器材加速器(TransMedx)。移師STB醫材開發...
連中岳:善用健保制定資料儲存標準,建置差異化影像資料庫
2021-03-11 / 記者 彭梓涵
現職為國立臺北護理健康大學資訊管理系暨研究所助理教授,同時也是社團法人台灣影像資訊標準化協會秘書長,專精醫學資訊系統、醫學影像儲存及傳輸系統(PACS)、醫學資訊通訊標準、資訊安全研究。曾參與臺灣DICOM標準的制定與協助臺灣加入國際DICOM協會。連中岳/社團法人台灣影像資訊標準化協會秘書長 責任編輯/彭梓涵電腦科技與資訊工業的進步與發展,對醫療帶來許多的革命,近年醫療器材不斷創新與改革,使各式...
Bluebird bio最新分析 基因療法LentiGlobin不會誘發白血病;類器官與疾病模型協會獲500萬歐元 助標準建立
2021-03-11 / 記者 彭梓涵
《美國》Bluebirdbio最新分析基因療法LentiGlobin不會誘發白血病美國時間10日,基因療法公司Bluebirdbio表示,近期在多項獨立的分析中證實,先前接受基因療法LentiGlobin治療鐮刀型血球貧血症(SCD),而罹患急性骨髓性白血病的(AML)患者,發現AML細胞中,慢病毒LVV載體插入在VAMP4基因或與囊泡相關的膜蛋白4(membraneprotein4)上,但Blu...
同時抑制3種VEGF受體! FDA批准AVEO晚期腎細胞癌新藥
2021-03-11 / 記者 彭梓涵
美國時間10日,製藥公司AVEOOncology宣布,美國食品藥物管理局(FDA)已批准其口服、每日一次血管內皮生長因子酪胺酸激酶抑制劑(VEGFR-TKI)--tivozanib,治療曾接受2種或更多種療法後復發/難治性晚期腎細胞癌(RCC)患者。消息一出,AVEO股價大漲90%。 此次批准主要是基於一項名為TIVO-3的三期試驗結果,在該試驗中,復發/難治性轉移性RCC患者,接受tivozan...
FDA批准KemPharm每日一次ADHD新型緩釋口服藥
2021-03-09 / 記者 彭梓涵
近(3)日,前驅藥物開發公司KemPharm宣布,開發的每日一次口服膠囊Azstarys,治療6歲以下注意力不集中(ADHD)兒童患者,獲得美國食品藥物管理局(FDA)批准。此為首款也是唯一款包含 d-MPH前驅藥物(Prodrug)的ADHD新型緩釋口服療法。 此次批准是基於一項多中心、雙盲、隨機、安慰劑對照組實驗。該研究招募了150位6-12歲被診斷為注意力不集中的患者進行研究,研究結果也顯示...