攜手推進BCMA CAR-T聯合療法
2017-12-11 / 記者 李虎門
致力於CAR-T療法開發的美國生技公司JunoTherapeutics日前宣佈,已與禮來(EliLillyandCompany)、OncoTracker以及FredHutchinso癌症研究中心簽署了三項授權合約,將推進其研發Anti-BCMACAR-T候選藥物聯合γ分泌酶抑制劑(GSIs)治療多發性骨髓瘤(MultipleMyeloma,MM)的臨床研究。一般而言,B細胞成熟抗原(B...
首個抗PD-1療法用於胃癌晚期治療 默克Keytruda 再獲FDA批准了
2017-09-25 / 記者 王柏豪
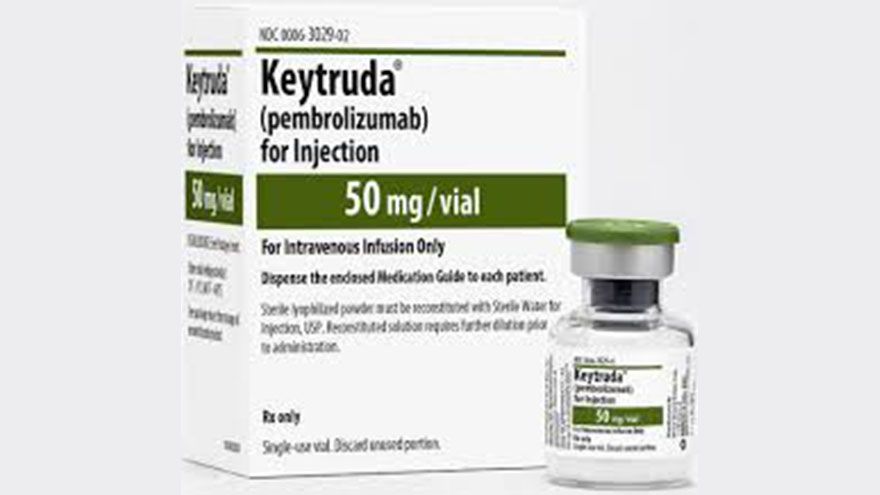
外電消息,FDA於美國時間23日又再度正式批准免疫療法新藥PD-1抗體Keytruda(pembrolizumab)用於治療罹患復發性局部晚期或轉移性胃癌/胃食管結合部腺癌,且腫瘤表達PD-L1的患者。這是美國FDA批准用於特定的胃癌患者人群的首款抗PD-1療法。默沙東的新藥研發人員們在一項名為KEYNOTE-059的臨床試驗中,進一步評估了Keytruda治療胃癌的潛力。該研究招募了259名患者...
PD-1/L1抑制劑安全仍存疑慮 FDA連叫停Roche、BMS、Merck臨床試驗
2017-09-20 / 記者 王柏豪
上週15日,製藥巨頭羅氏(Roche)宣佈FDA要求暫停(已入組或經治療獲益的患者依然可以繼續)目前進行的Tecentriq(Atezolizumab,阿特珠單抗)與Pomalyst(pomalidomide,泊馬度胺)(Ib/II)\Revlimid(lenalidomide,來那度胺)(Ib)聯合治療復發或難治型多發性骨髓瘤的臨床試驗,目的是要調查免疫檢查點抑制劑與患者死亡之間的關係。FDA在...
癌症救星免疫治療 產業投資需謹慎
2017-08-24 / 記者 林以璿
現今免疫療法藥物的開發,在全球被推向了浪潮的最高峰。然而,腫瘤免疫療法真的是未來的趨勢嗎?元富證券攜手環球生技,邀請震泰生醫執行長李冬陽、台大醫院內科部免疫風溼科主治醫師許秉寧,以及生技中心企劃管考室主任寇怡衡,針對腫瘤免疫治療,提出醫學上與投資上的未來預測。台大醫院內科部免疫風溼科主治醫師許秉寧表示,免疫療法並不是新的概念,但一直要到找到了靶點,免疫療法才終於不再是神話。「免疫療法是可行的,但不...
強強聯手 阿斯特捷利康與默克合作藥物開發
2017-08-03 / 記者 李虎門
英國製藥龍頭阿斯特捷利康(AstraZeneca)宣佈,將與美國默克(Merck)合作、共同開發阿斯特捷利康旗下標靶藥物Lynparza(olaparib)和selumetinib,期望能夠加速藥物商品化的腳步。Lynparza是一種PARP(多聚ADP核糖聚合酶)抑制劑,早於2014年底,美國和歐盟已經批准上市,並運用在晚期卵巢癌接受多種療法但失敗的BRCA突變(BRCA-mutated)患者。...